问题
问答题
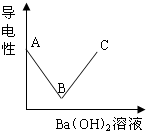
右图表示向硫酸溶液中水滴加氢氧化钡溶液发生中和反应时,溶液导电性的变体.
试解释:
(1)B表示______;
(2)由A到B导电性降低的原因是______;
(3)由B到C导电性升高的原因是______.
答案
根据化学知识:向一定量的稀硫酸中逐渐滴入氢氧化钡溶液,将得到硫酸钡沉淀,导电性变弱,即为图中AB段所示;B点是两者恰好完全中和,溶液中基本上无自由移动的离子,故导电性最小;当滴入氢氧化钡溶液过量时,硫酸用完,只剩下氢氧化钡溶液,随着氢氧化钡的逐渐增多,离子浓度逐渐增大,导电性会增强.
故答案为:(1)B点是两者恰好完全中和,溶液中基本上无自由移动的离子,故导电性最小;
(2)硫酸溶液和氢氧化钡溶液发生了中和反应,生成的BaSO4又难溶于水,溶液中的离子浓度逐渐降低;
(3)两者恰好完全中和后,由于加入的Ba(OH)2渐多,溶液中的离子浓度逐渐增大,所以导电性又逐渐升高.
