现有HCl、NaCl、NaOH、Na2CO3等溶液.若进行下列实验,请判断可能的溶液组合.
(1)两两组合进行实验:
①组合后无明显现象,但发生反应的组合是______;
写出该反应的化学方程式为______.
②组合后有明显现象,该现象是______.
反应的化学方程式为______.
(2)任意组合进行实验:
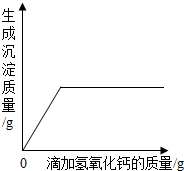
若将氢氧化钙溶液逐滴滴入组合溶液中,产生的沉淀与加入的氢氧化钙有如图所示的关系,则溶液的组合可能是______.
①HCl和NaOH、混合后无明显现象,因在溶液中反应生成水,看不到现象,但发生了化学反应,有关的化学方程式为:HCl+NaOH=NaCl+H2O;
故答案为:NaOH、HCl;NaOH+HCl═NaCl+H2O
②溶液中的反应现象是生成气体、沉淀或溶液变色;根据以上物质HCl和Na2CO3反应生成氯化钠、水和二氧化碳,生成的二氧化碳逸出,有气泡产生.
故答案为:有气泡产生、Na2CO3+2HCl═2NaCl+H2O+CO2↑
(2)氢氧化钙溶液只与以上物质中的碳酸钠反应生成沉淀,故其溶液中一定含有碳酸钠;因含有碳酸钠则组合溶液中不含有与碳酸钠能反应的氯化氢;则组合溶液应是Na2CO3与NaCl、NaOH之间的组合;
故答案为:①Na2CO3和NaOH、②Na2CO3和NaCl、③Na2CO3、NaOH和NaCl

