(19分)在常温下,Fe与水并不起反应,但在高温下,Fe与水蒸气可发生反应。 应用下列装置,在硬质玻璃管中放入还原铁粉和石棉绒的混合物,加热,并通入水蒸气,就可以完成高温下“Fe与水蒸气的反应实验”。请回答该实验中的问题。

(1)写出该反应的化学方程式 ,其中氧化剂是 ,还原剂是 。8.4g铁粉参加反应,转移电子 mol。
(2)玻璃管中石棉绒的作用是 ,实验开始时应先点燃 ,实验结束时应先熄灭 。
(3)圆底烧瓶中盛装的水,该装置受热后的主要作用是 ;烧瓶里应事先放置 ,其作用是 。
(4)该同学欲确定反应后硬质试管中固体物质的成分,设计了如下实验方案:
①待硬质试管冷却后,取少许其中的固体物质溶于稀硫酸得溶液B;
②取少量溶液B滴加KSCN溶液,若溶液变红色则说明硬质试管中固体物质的
成分是 ,若溶液未变红色则说明硬质试管中固体物质的
成分是 。
(5)该同学按上述实验方案进行了实验,结果溶液未变红色,原因是
(用离子方程式表示)。

(6)该同学马上另取少量溶液B,使其跟NaOH溶液反应。若按上图所示的操作,可观察到生成白色沉淀,迅速变成灰绿色,最后变成红褐色的现象,请写出与上述现象相关
的反应的化学方程式 ,
。
(7)一段时间后,该同学发现(4)中未变红的溶液变成红色,说明Fe2+ 具有 性。由此可知,实验室中含Fe2+的盐溶液现用现配制的原因是 ,
并且配制含Fe2+的盐溶液时应加入少量 。
(1)3Fe+4H2O(g) 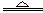 Fe 3O4 +4 H2(不写(g)或“加热”扣1分,写成“高温”不扣分)
Fe 3O4 +4 H2(不写(g)或“加热”扣1分,写成“高温”不扣分)
H2O Fe 0.4
(2)铁粉的载体,增大铁粉与水蒸气的接触面积 酒精灯 酒精喷灯
(3)为实验提供水蒸气 碎瓷片 防止暴沸
(4)一定有Fe3O4,可能有Fe(各1分) Fe3O4和Fe
(5)Fe + 2Fe3+= 3Fe2+
(6)FeSO4 + 2NaOH = Fe(OH)2↓+ Na2SO4(1分)
4Fe(OH)2 + O2 + 2H2O = 4Fe(OH)3(1分)
(7)还原 Fe2+易被空气中的氧气氧化而变质 铁粉
