用10mol/L 浓硫酸配制50 ml 1.0mol/L稀硫酸,若实验仪器有:
A.25mL量筒 B.托盘天平 C.玻璃棒 D.50mL容量瓶
E.10mL量筒 F.胶头滴管 G.50mL烧杯 H.100mL容量瓶
(1)需量取浓硫酸的体积为 mL。
(2)实验时选用的仪器有(填序号) 。
(3)在容量瓶使用方法中,下列操作正确的是(填序号) 。
A.使用容量瓶前检查它是否漏水
B.容量瓶用蒸馏水洗净后,再用待配液润洗
C.将准确量取的10mol/L的硫酸,注入已盛有20mL水的50mL的容量瓶中,加水至刻度线
D.定容后塞好瓶塞,用食指顶住瓶塞,用另一只手的手指托住瓶底,把容量瓶倒转摇匀
(4)下列情况对所配制的稀硫酸浓度有何影响?(用偏大、偏小、无影响填写)
A. 未冷却至室温就注入容量瓶中定容
B. 容量瓶用蒸馏洗涤后残留有少量的水
C. 所用过的烧杯、玻璃棒未洗涤
D. 定容时仰视溶液的凹液面
1) 5 mL。 (2分)(2) CDEFG 。(4分)(3) AD 。(4分)
(4)A. 偏大 B. 无影响 C. 偏小 D. 偏小 (8分)
考查一定物质的量浓度的配制。
(1)硫酸在稀释过程中,溶质的物质的量是不变的,所以需要浓硫酸的体积是
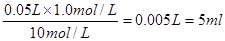 。
。
(2)浓硫酸是液体,不能称量,而要用量筒量取。浓硫酸需要5ml,所以选择规格最近的10魔力量筒。溶解需要烧杯,玻璃棒,定容还需要胶头滴管,所以答案是CDEFG。
(3)容量瓶不能用标准液润洗,否则结果偏高,B不正确。稀释浓硫酸不应在容量瓶中进行,而应该在烧杯中,C不正确。AD都是正确的,所以正确的答案是AD。
(4)根据热胀冷缩可知,如果没有冷却就定容,则容量瓶中溶液体积偏小,测定结果就偏大。容量瓶中残留蒸馏水,对结果没有影响。未洗涤烧杯玻璃棒等,会导致溶质偏小,测定结果偏小。定容时仰视刻度线,则溶液的体积偏大,测定结果偏小。
