为验证并除去NaCl晶体中含有少量的Na2CO3和Na2SO4两种杂质,现设计了如下实验方案(通过查阅相关资料得知:若两种盐溶液混合,有沉淀产生,则该复分解反应可以发生).
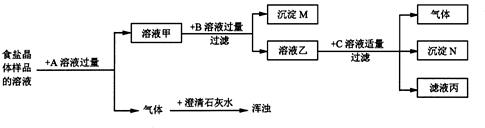
请回答:
用化学式填写:M______,B______,C______,N______;溶液甲中一定含有的物质是______.
(1)因为要验证并除去食盐晶体中含有少量的Na2CO3和Na2SO4两种杂质,实质就是除去碳酸根和硫酸根,在不带入其他杂质的基础上,除碳酸根用盐酸,除硫酸根用氯化钡,为了彻底的把杂质离子除去,加入的某些除杂剂要过量.根据加入溶液A后会生成气体,而混合物中有碳酸钠,可以知道加入了酸,但是反应后又不能引入新的杂质,所以要加盐酸,溶液甲中含有硫酸根,可加入过量的氯化钡除去,生成的沉淀M就是硫酸钡,溶液乙中含有剩余的盐酸和氯化钡,可加入适量的碳酸钠一次除去,生成的气体是二氧化碳,沉淀N是碳酸钡,滤液丙就是氯化钠溶液;故M是BaSO4;B是BaCl2;C是 Na2CO3; N是BaCO3;
(2)加过量的盐酸反应后,除去了碳酸钠,溶液中有氯化钠和剩余的盐酸还有硫酸钠,即:Na2SO4、NaCl、HCl;
故答案为:BaSO4; BaCl2; Na2CO3; BaCO3; Na2SO4、NaCl、HCl.
