(7分)构成物质的粒子之间的关系如右图所示。
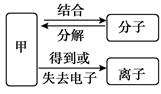
(1)甲是 。
(2)氧气、汞和氯化钠3种物质中,由离子构成的是 。
(3)某粒子的结构示意图为 。
。
① 当a= 时,该粒子是原子;② 当a=11时,该粒子的符号为 。
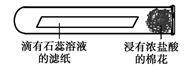
(4)如右图所示,将滴有石蕊溶液的滤纸放入试管中,试管口放置一浸有浓盐酸的棉花,可观察到的现象是 , 此现象说明分子具有的性质是 。
(5)下图为某反应的部分微观示意图,其中不同的球代表不同元素的原子。
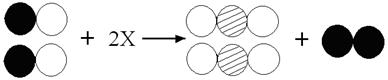
请画出X分子的微观示意图: 。
(1)原子 (2)氯化钠 (3)① 10 ② Na+
(4)滴有石蕊的滤纸变红 分子是不断运动的 (5)
题目分析:(1)分子是由原子构成的,原子得失电子可形成离子,故甲为原子;
(2)氧气是由氧分子构成的,汞是由汞原子构成的,氯化钠是由氯离子和钠离子构成的;
(3)①在原子中,核电荷数=质子数=核外电子数,故a=10;
②当a=11时,核外电子数比核内质子数少1,为带一个单位正电荷的阳离子,根据离子符号的表示法:在元素符号的右上角标明离子所带电荷数及电性,则为Na+。
(4)分子是在不断运动着的,而由于浓盐酸具有挥发性,即氯化氢分子比石蕊分子运动的快,且石蕊试液遇显酸性的溶液变红,故当氯化氢分子遇到石蕊试液时,能使滴有石蕊的滤纸变红。
(5)根据质量守恒定律,在化学反应中,反应前后原子的种类没有改变,数目没有增减,而反应前有黑球2个,白球2个,反应后黑球2个,白球4个,花球2个,故可知2X中含有白球2个,花球2个,则X中含有白球1个,花球1个,由此可推测出X分子的微观示意图为 。
。
点评:理解分子、原子、离子都是构成物质的基本微粒,掌握它们之间的相互转换关系,并能灵活运用质量守恒定律,是解题的关键。
