Ⅰ、高纯MnCO3是制备高性能磁性材料的主要原料。实验室以MnO2为原料制备少量高纯MnCO3的操作步骤如下:
(1)制备MnSO4溶液:在烧瓶中(装置见图)加入一定量MnO2 和水,搅拌,通入 SO2和N2混合气体,反应3h。停止通入SO2,继续反应片刻,过滤(已知MnO2+H2SO3=MnSO4+H2O)。
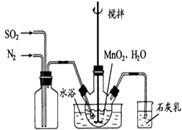
①石灰乳作用: 。
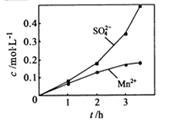
②若实验中将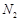 换成空气,测得反应液中Mn2+、SO42-的浓度随反应时间t变化如右图。导致溶液中Mn2+、SO42-浓度变化产生明显差异的原因是 。
换成空气,测得反应液中Mn2+、SO42-的浓度随反应时间t变化如右图。导致溶液中Mn2+、SO42-浓度变化产生明显差异的原因是 。
(2)制备高纯MnCO3固体:已知MnCO3难溶于水、乙醇,潮湿时易被空气氧化,100℃开始分解;Mn(OH)2开始沉淀时pH="7.7," 请补充由(1)制得的MnSO4溶液制备高纯MnCO3的操作步骤:
[实验中可选用的试剂:Ca(OH)2、NaHCO3、Na2CO3、C2H5OH]。
① ;
② ;
③检验SO42-是否被洗涤除去; ④用少量乙醇洗涤; ⑤低于100℃干燥。
Ⅱ、锌铝合金的主要成分有Zn、Al、Cu、Si等元素。实验室测定其中Cu含量的步骤如下:①称取该合金样品1.1g,用HCl和H2O2溶解后,煮沸除去过量H2O2,过滤,滤液定容于250mL容量瓶中。
②用移液管移取50.00mL滤液于250mL碘量瓶中,控制溶液的pH=3~4,加入过量KI溶液(生成CuI和I2)和指示剂,用0.01100mol×L-1Na2S2O3溶液滴定生成的I2至终点(反应:I2 + 2S2O32- = 2I- + S4O62-),消耗Na2S2O3溶液6.45mL。
(1)判断步骤②滴定终点的方法是 。
(2)计算合金中Cu的质量分数 。
Ⅰ、(1)①吸收多余的二氧化硫(1分)②O2与H2SO3反应生成H2S04(1分)
(2)①边搅拌边加入NaHCO3(Na2CO3),并控制溶液pH<7.7 (2分)②过滤,用少量水洗涤2~3次。(2分)
Ⅱ、(1)当滴入最后一滴Na2S2O3溶液时,溶液由蓝色突变为无色,且半分钟不变色(2分) (2)0.02064(2分)
Ⅰ、(1)①由于SO2是大气污染物,需要尾气处理,即石灰乳的作用是吸收多余的二氧化硫。
②由于氧气具有氧化性,而亚硫酸具有还原性,因此原因是O2与H2SO3反应生成H2S04导致的。
(2)要生成碳酸锰,则需要加入碳酸盐,然后通过控制溶液的pH即可产生碳酸锰。碳酸锰不溶于水,过滤得到,即步骤是①边搅拌边加入NaHCO3(Na2CO3),并控制溶液pH<7.7 (2分)②过滤,用少量水洗涤2~3次。
Ⅱ、(1)①由于碘遇淀粉显蓝色,所以指示剂是淀粉,终点时的现象是当滴入最后一滴Na2S2O3溶液时,溶液由蓝色突变为无色,且半分钟不变色。
②铜离子氧化碘离子的方程式为2Cu2++4I-=2CuI+I2,因此根据I2 + 2S2O32- = 2I- + S4O62-可知,Cu2+~S2O32-。所以铜离子的物质的量是0.01100mol/L×0.00645L=7.095×10-5mol,则合金中铜的质量是7.095×10-5mol×5×64g/mol=0.022704g,所以质量分数是0.022704÷1.1=0.02064。
