(12分)用18 mol·L-1浓硫酸配制100 mL 3.0 mol·L-1稀硫酸的实验步骤如下:
①计算所用浓硫酸的体积 ②量取一定体积的浓硫酸③溶解 ④转移、洗涤 ⑤定容、摇匀完成下列问题:
(1)所需浓硫酸的体积是________,量取浓硫酸所用的量筒的规格是________
(从下列中选用A.10 mL B.25 mL C.50 mL D.100 mL)。
(2)第③步实验的操作是__________________________ 。
(3)第⑤步实验的操作是________________ 。
(4)下列情况对所配制的稀硫酸浓度有何影响?(用“偏大”“偏小”“无影响”填写)
A.所用的浓硫酸长时间放置在密封不好的容器中___________________
B.容量瓶用蒸馏洗涤后残留有少量的水________________
C.所用过的烧杯、玻璃棒未洗涤________________
D.定容时俯视刻度线________________
(1)16.7ml B
(2)先向烧杯加入30ml(或适量)蒸馏水,然后将浓硫酸沿烧杯内壁缓慢倒入烧杯中,并用玻璃棒搅拌
(3)继续向容量瓶注入蒸馏水至离刻度线1-2cm处,改用胶头滴管向容量瓶滴加至液凹面与刻度线相切为止、塞进瓶塞,反复颠倒摇匀
(4)A.偏小 B.无影响 C.偏小 D.偏大
(1)根据稀释过程中溶质不变可知,需要浓硫酸的体积是
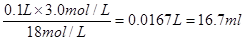 。量筒的规格越近16.7ml,误差越小,所以选择的量筒是25ml的,即答案选B。
。量筒的规格越近16.7ml,误差越小,所以选择的量筒是25ml的,即答案选B。
(2)浓硫酸溶于水放出大量的热,且硫酸的密度大于水的,所以稀释浓硫酸的正确操作是:先向烧杯加入30ml(或适量)蒸馏水,然后将浓硫酸沿烧杯内壁缓慢倒入烧杯中,并用玻璃棒搅拌。
(3)定容时需要胶头滴管,所以正确的操作是:继续向容量瓶注入蒸馏水至离刻度线1-2cm处,改用胶头滴管向容量瓶滴加至液凹面与刻度线相切为止、塞进瓶塞,反复颠倒摇匀。
(4)根据c=n/V可知,浓硫酸具有吸水性,长时间放置,浓度变稀,配制的浓度就偏小;容量瓶中含有蒸馏水,不影响配制的浓度;烧杯、玻璃棒没有洗涤,则溶质减少,浓度偏低;定容时俯视刻度线,则容量瓶中溶液的体积偏少,则浓度偏大。
