(14分,每空2分)某课外小组利用H2还原黄色的WO3粉末测定W的相对原子质量,下图是测定装置的示意图,A中的试剂是盐酸。
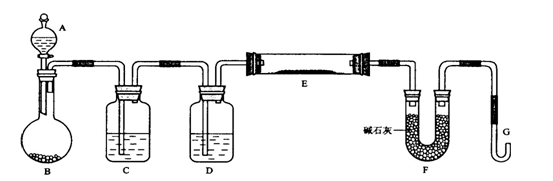
请回答下列问题。
(1)仪器中装入的试剂:C________ 、 D________;
(2)连接好装置后应首先____________________;
(3)“加热反应管E(用“H”表示)”和“从A瓶逐滴滴加液体(用“I”表示)”这两步操作应该先进行的是(用“H”或“I”表示)_____________。在这两步之间还应进行的操作是_____________________;
(4)从实验中测得了下列数据
①空E管的质量a ②E管和WO3的总质量b
③反应后E管和W粉的总质量c(充分反应后冷却到室温称量)
④反应前F管及内盛物的总质量d ⑤反应后F管及内盛物的总质量e
由以上数据可以列出计算W的相对原子质量的不含“c”字母的一个计算式(可以不写单位。除W外,其他涉及的元素的相对原子质量均为已知):
计算式:Ar(W)=____________;
(5)此实验除了要对G口余气作处理外,似还有待改正之处,否则会引起较大的误差,你认为应该作何改正?________________________ 。
(1)水 H2SO4(浓)
(2)检查装置的气密性
(3)Ⅰ;检验H2的纯度
(4)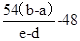 (凡写
(凡写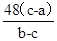 或
或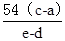 的不给分)
的不给分)
(5)在G管出口处点燃除去尾气
(1)B、C、D装置是制取干燥、纯净的氢气,故B中应是锌粒,C中应是除HCl的H2O,D中应是除去H2O的浓硫酸;
(2))连接好装置后应首先检验装置的气密性:检密要注意三步:第一步先封闭气体,第二步对封闭气体改变压强,第三步说出对应现象。
(3)装置E需要加热,而氢气若与空气混合加热易爆炸,故应先从A瓶逐滴滴加液体制取氢气,用制取的氢气将装置中的空气排尽,检验H2的纯度后再加热;
(4)设W的原子量为M,则
由WO3 + 3H2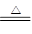 W + 3H2O
W + 3H2O
M+48 54
b—a e—d
可求出:M=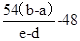
(5)在E中反应后产生水蒸气和未反应的氢气通入到F中,在F中碱石灰吸收水蒸气,则在G管逸出的气体是未反应的氢气;由于氢气具有可燃性,可在G管出口处点燃;
