问题
计算题
(6分)氢气还原氧化铜的反应不完全时,便得到Cu、Cu2O、CuO的固体混合物。化学兴趣小组同学为探究上述固体的成分进行了如下操作和实验:
(1)取一定质量的均匀固体混合物A,将其分成两等份。
(2)取其中—份用足量的氢气还原,测得反应后固体质量减少3.20g。
(3)另一份加入500mL稀硝酸,固体恰好完全溶解,且同时收集到标准状况下NO气体2.24L。
请回答以下问题:
(1)A中,n(CuO)+n(Cu2O)= 。
(2)A中,n(CuO)的取值范围是 。
(3)试计算所用稀硝酸的物质的量浓度_______________。
答案
(1) n(Cu)+n(Cu2O)="0.300mol " (2)0.1mol<n(CuO)<0.4mol
(3)设其中一份中n(Cu)= x mol,n(Cu2O)=" y" mol,n(CuO)=" z" mol,
依得失电子守恒和氧元素守恒,有: 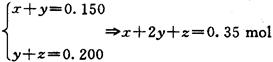
亦即反应后生成的硝酸铜的物质的量为0.350mol
则500mL稀硝酸中,n(HNO3)=0.350mol×2+0.100mol=0.800mol)
于是:c(HNO3)=0.800mol/0.500L=1.6mol/L
