(10分)某氯化铁样品含有FeCl2杂质。现要测定其中铁元素的质量分数,实验按以下步骤进行:
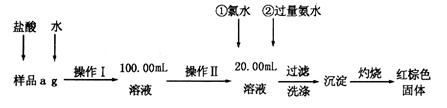
(1)操作I所用到的玻璃仪器除烧杯、玻璃棒外,还必须有________________________(填仪器名称)。
(2)写出加入氯水发生反应的离子方程式____________________。
(3)检验沉淀已经洗涤干净的操作及现象是______________________________________
___________________________________________________________________________。
(4)坩埚质量为W1g,加热后坩埚与红棕色固体总质量为W2g,则样品中铁元素的质量分数是____________________(列出原始算式,不需化简);若称量准确而最终测量的结果偏大,则造成误差的原因可能是_____________________(写出一种原因即可)。

题目分析:(1)溶液的配制还需要100ml容量瓶和胶体滴管,需要注意的是容量瓶必须注明100ml。
(2)加入氯水后,Cl2把Fe2+氧化为Fe3+。
(3)如果未洗涤干净,沉淀表面含有NH4Cl,所以用AgNO3检验出最后一次洗涤液无Cl‾即可。
(4)灼烧后得到的固体为Fe2O3,质量为W2-W1,可算出Fe元素的质量为:112(W2-W1)/160,因为原样品配制了100.00ml溶液,从中取出了20.00ml进行的实验,所以乘以5得原样品中铁元素的质量,进而求出质量分数。
