孔雀石的主要成分为Cu2(OH)2CO3,还含少量铁的氧化物和硅的氧化物。以下是实
验室以孔雀石为原料制备CuSO4·5H2O晶体的流程图:

(1)研磨孔雀石的目的是 。浸泡孔雀石的试剂A若选用过量的稀硫酸,则固体a是 (填化学式)。
(2)试剂B的目的是将溶液中的Fe2+转化为Fe3+,则试剂B宜选用 (填序号):
A.酸性KMnO4溶液 B.双氧水 C.浓硝酸 D.氯水
相应的离子方程式为: 。
(3)试剂C用于调节溶液pH,使Fe3+转化为沉淀予以分离。则试剂C宜选用 (填序号):
A.稀硫酸 B.NaOH溶液 C.氨水 D.CuO
固体C的化学式为 。
(4)1 mol氨气通过加热的Cu2(OH)2 CO3可以产生1.5 mol金属铜,则该反应的化学方程式为 。
(5)常温下Fe(OH)3的Ksp=1×10-39,若要将溶液中的Fe3+转化为Fe(OH)3沉淀,使溶液中c(Fe3+)降低至1×10—3 mol/L,必需将溶液调节至pH= 。
(1)(共4分)增大固体表面积(1分),以增大反应速率(1分)[类似意思均可]
SiO2(2分)
(2)(共4分)B(2分) 2Fe2++2H++H2O2=2Fe3++2H2O(2分)(未配平1分,写为化学方程式2FeSO4 + H2SO4 + H2O2 = Fe2(SO4)3 + 2H2O且正确1分)
(3)(共4分)D(2分) Fe(OH)3(2分)
(4)(共3分)3Cu2(OH)2CO3 + 4NH3 6Cu + 3CO2 + 9H2O +2 N2(化学式1分、配平均1分,条件1分。)
6Cu + 3CO2 + 9H2O +2 N2(化学式1分、配平均1分,条件1分。)
(5)(共2分)2
题目分析:(1)研磨孔雀石的目的是为了酸溶速率更快,所以答案为“增大固体接触面积,加快反应速率”,酸溶过程中不溶的固体为杂质SiO2。
(2)把Fe2+转化为Fe3+ 应该加入氧化剂,且不能带入杂质离子,所以用双氧水,选B。相应的离子方程式为:2Fe2++2H++H2O2=2Fe3++2H2O。
(3)因为目标产品是CuSO4·5H2O晶体,所以调节pH值使铁离子沉淀应选用的试剂不能带入杂质离子,所以选用固体CuO,所以沉淀物c为Fe(OH)3 和过量的CuO。
(4)碱式碳酸铜中通入氨气后有铜单质生成,说明铜被还原,NH3做还原剂。因为1mol氨气还原得到1.5mol铜单质,根据铜+2→0价,可知转移电子3mol,得失电子守恒,所以NH3失去电子也为3mol,所以可推测得NH3被氧化为了N2,所以可以得知其他产物还有CO2、H2O。所以列出反应物NH3+ Cu2(OH)2 CO3→Cu+ N2+CO2+H2O,然后根据氧化还原反应方程式配平得:3Cu2(OH)2CO3 + 4NH3 6Cu + 3CO2 + 9H2O +2 N2 。
6Cu + 3CO2 + 9H2O +2 N2 。
(5)根据Fe(OH)3溶解平衡Fe(OH)3 (s)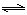 Fe3+ (aq)+3 OH- (aq)可得Ksp ="c(" Fe3+ ) ·c3(OH- )= 1×10-39 ,所以把c(Fe3+)=1×10—3 mol/L带入公式中,计算得c(OH- )= 1×10-12 ,所以c(H+ )="Kw/" c(OH- )= 10-2 ,所以pH=2。
Fe3+ (aq)+3 OH- (aq)可得Ksp ="c(" Fe3+ ) ·c3(OH- )= 1×10-39 ,所以把c(Fe3+)=1×10—3 mol/L带入公式中,计算得c(OH- )= 1×10-12 ,所以c(H+ )="Kw/" c(OH- )= 10-2 ,所以pH=2。
