问题
选择题
铁和氧化铁的混合物共a mol,加盐酸后固体全部溶解,共收集到b mol氢气,且向反应后的溶液中加入KSCN溶液不显红色,则原混合物中单质铁的物质的量为 ( )
A. (a+b) mol
(a+b) mol
B.(a-b) mol
C. (a-b)mol
(a-b)mol
D.(a+b) mol
答案
答案:A
题目分析:发生的反应为:①Fe2O3+6HCl=2FeCl3+3H2O; ②2FeCl3+Fe=3FeCl2. ③Fe+2HCl= FeCl2+H2↑.由于向反应后的溶液中加入KSCN溶液不显红色,说明溶液中不含有Fe3+.完全为Fe2+.由③可得Fe-- H2。n(H2)=n(Fe)=bmol,,则还有 (a-b)mol.由①②可得Fe2O3---2FeCl3----Fe可知发生该反应的Fe的物质的量为(a-b)mol÷2="(a-b)/2" mol因此在固体混合物中的铁粉的物质的量为bmol+(a-b)/2 mol=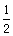 (a+b) mol。所以选项为A。2O3、Fe的化学性质及Fe3+的检验的知识。
(a+b) mol。所以选项为A。2O3、Fe的化学性质及Fe3+的检验的知识。
