电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板。
(1)FeCl3溶液与金属铜发生反应的离子方程式是 。
(2)检验溶液中Fe3+存在的操作步骤和现象是 。
(3)某工程师为了从使用过的腐蚀废液中回收铜,并重新获得氯化铁溶液,准备采用下列步骤:
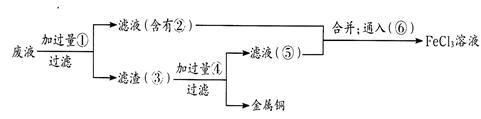
上述实验中加入或生成的有关物质的化学式为② ④____________
通入⑥得到FeCl3溶液的离子反应方程式为________________。
(1)2Fe3++Cu=2Fe2++Cu2+(2)取少许溶液,向其中滴加KSCN溶液,溶液变红色 (其他合理答案同样得分)(3)②FeCl2 ④ HC1 2Fe2++C12=2Fe3++2C1–
题目分析:(1)FeCl3溶液与金属铜发生反应生成氯化亚铁和氯化铜,离子方程式是2Fe3++Cu=2Fe2++Cu2+;(2)检验溶液中Fe3+存在通常用KSCN溶液,操作步骤和现象是取少许溶液,向其中滴加KSCN溶液,溶液变红色;(3)反应的废液中含有氯化亚铁、氯化铜,由工艺流程可知,废液中加入过量①铁粉发生反应Fe+Cu2+=Fe2++Cu,过滤得滤液为氯化亚铁溶液,滤渣③为金属铜和铁的混合物,滤渣③加入过量盐酸,发生反应Fe+ 2HC1=FeC12+H2,过滤得金属铜,滤液为氯化亚铁溶液,氯化亚铁溶液中通入氯气发生反应2Fe2++C12=2Fe3++2C1–,可以得到氯化铁。根据上述分析知,②为FeCl2,④为HC1;通入⑥得到FeCl3溶液的离子反应方程式为2Fe2++C12=2Fe3++2C1– 。
