氯化铜、氯化亚铜是重要的化工原料,广泛地用作有机合成催化剂。
I.实验室中以粗铜(含杂质Fe)为原料制备铜的氯化物。现用如图所示的实验仪器及药品来制备纯净、干燥的氯气并与粗铜反应(铁架台、铁夹、酒精灯已省略)。按要求回答下列问题:
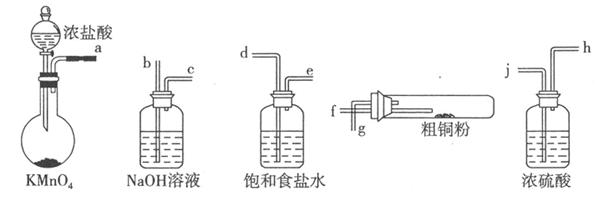
(1)按气流方向连接各仪器接口顺序是:a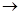 、
、 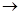 、
、 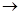 、
、 
(2)写出加热时硬质试管中发生化学反应的方程式是 。
(3)反应后,盛有NaOH溶液的广口瓶中溶液具有漂白、消毒作用,若用钢铁(含Fe、C)制品盛装该溶液会发生电化腐蚀,钢铁制品表面生成红褐色沉淀,溶液会失去漂白、杀菌消毒功效。该电化腐蚀过程中正极反应式是 .
II.将上述实验制得的固体产物按如下流程操作,试回答下列问题:
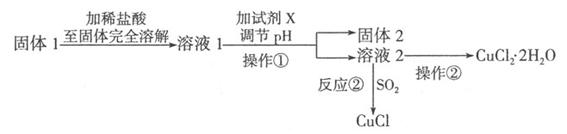
(1)检验溶液2中是否含有杂质离子的试剂是 ;
(2)某同学用实验制得的CuCl2·2H2O晶体配制0.1 mol·L-1的CuCl2溶液,在称量出CuCl2·2H2O晶体后,溶解该晶体的具体操作为
(3)溶液l可加试剂X用于调节pH以除去杂质,X可选用下列试剂中的(填序号)
a.NaOH b.NH3·H2O C.CuO d.CuSO4 e.Cu2(OH)2CO3
(4)反应②是向溶液2中通入一定量的SO2,加热一段时间后生成CuCl白色沉淀。写出制备CuCl的离子方程式: .
Ⅰ:(1)d e j h f g b(3分)(2)Cu+Cl2 CuCl2,(2分)2Fe+3Cl2
CuCl2,(2分)2Fe+3Cl2 2FeCl3(2分)(3)ClO-+2e-+H2O=Cl-+2OH-(2分)(2分)Ⅱ:(1)KSCN溶液;(2分)(2)将称量的晶体置于烧杯中,加入适量的稀盐酸和蒸馏水,用玻璃棒搅拌(3分)(3)c、e(2分)(4)2Cu2++2Cl-+SO2+2H2O
2FeCl3(2分)(3)ClO-+2e-+H2O=Cl-+2OH-(2分)(2分)Ⅱ:(1)KSCN溶液;(2分)(2)将称量的晶体置于烧杯中,加入适量的稀盐酸和蒸馏水,用玻璃棒搅拌(3分)(3)c、e(2分)(4)2Cu2++2Cl-+SO2+2H2O 2CuCl↓+4H++SO42-(3分)
2CuCl↓+4H++SO42-(3分)
试题解析:(1)制得的氯气先通过饱和食盐水除去氯化氢气体,再通过浓硫酸除水,然后再通入粗铜中,最后进行尾气处理。(2)在硬质试管中铜和铁都与氯气反应;(3)根据题目信息可知,电池反应应该为铁和次氯酸钠反应,故正极为次氯酸根得电子生成氯离子。Ⅱ:(1)固体1中加入盐酸反应后溶液中含有铁离子、铜离子和亚铁离子,加入试剂目的是把亚铁离子氧化成铁离子,调节pH使铁离子水解生成沉淀而除去,故溶液2中的杂质离子为铁离子,加入KSCN溶液检验;(2)溶解氯化铜时要加入盐酸抑制铜离子的水解;(3)加入的试剂X能与氢离子反应调节pH而又不能引入新的杂质,故选择c和e;(4)根据已知信息铜离子和二氧化硫反应生成CuCl,铜离子发生还原反应,二氧化硫被氧化成硫酸根离子,再依据离子方程式中的电荷守恒和原子守恒得离子方程式。
