某氯化铁样品含有少量FeCl2杂质。现要测定其中铁元素的质量分数,实验按以下步骤进行:
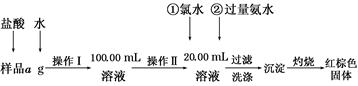
(1)操作Ⅰ所用到的玻璃仪器除烧杯、玻璃棒外,还必须有________、________(填仪器名称)。
(2)写出加入氯水发生反应的离子方程式_____________________________________。
(3)检验沉淀已经洗涤干净的操作及现象是_____________________。
(4)坩埚质量为W1 g,加热后坩埚与红棕色固体总质量为W2 g,则样品中铁元素的质量分数是________ (列出原始算式,不需化简);若称量准确而最终测量的结果偏大,则造成误差的原因可能是_____________________________________________________________
(写出一种原因即可)。
(1)100 mL容量瓶、胶头滴管
(2)2Fe2++Cl2=2Fe3++2Cl-
(3)取少量最后一次洗涤液,滴加AgNO3溶液,若无沉淀生成,则证明洗涤干净;
(4) ×100% 固体加热时未充分反应变为Fe2O3
×100% 固体加热时未充分反应变为Fe2O3
(1)配制100 mL溶液,需用100 mL容量瓶,定容时使用胶头滴管;(2)氯气有强氧化性,能把二价铁离子氧化生成三价铁离子同时生成氯离子,离子方程式为2Fe2++Cl2=2Fe3++2Cl-。(3)检验沉淀已洗涤干净时,取少量最后一次洗涤液,滴加AgNO3溶液,若无沉淀生成,则证明洗涤干净;(4)红棕色固体是氧化铁,其质量是W2 g-W1 g,其中铁元素的质量是 g,样品中铁元素的质量分数是
g,样品中铁元素的质量分数是 ×100%;固体加热时未充分反应变为Fe2O3会导致测量结果偏大。
×100%;固体加热时未充分反应变为Fe2O3会导致测量结果偏大。
