问题
问答题
试样X由氧化亚铁和氧化铜组成.取质量相等的两份试样按下图所示进行实验:
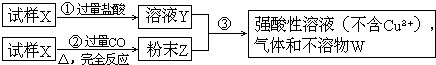
(1)请写出步骤③中所发生的全部反应的离子方程式.
(2)若全部的溶液Y和全部的粉末Z充分反应后,生成的不溶物W的质量是m,则每份试样X中氧化铜的质量为______.(用m表示)
答案
(1)因为CuO+CO
Cu+CO2,FeO+CO 加热 .
Fe+CO2,所以固体粉末Z为Cu和Fe.铁能和铜离子发生置换反应,所以铁和铜离子发生的离子方程式为:Fe+Cu2+=Cu+Fe2+;强酸性溶液E不含铜离子,且有气体F生成,所以铁与铜离子反应铁过量,铁还和酸反应,所以铁和酸反应的离子方程式为:Fe+2H+=Fe2++H2↑; 加热 .
答:步骤③中所发生的全部反应的离子方程式为Fe+Cu2+=Cu+Fe2+、Fe+2H+=Fe2++H2↑;
(2)不溶物W为铜,铜有两部分来源,一部分是CO还原出的铜,一部分为铁与铜离子反应置换出的铜,所以以W的一半计算试样中的氧化铜的质量;
CuO--Cu
80g 64g
m m5 4
所以试样中氧化铜的质量为
m×5 4
=1 2
m,故答案为:5 8
m.5 8
