铜是人类最早生产和使用的金属之一,在化学反应中铜元素可表现为0、+1、+2价。
Ⅰ.(1)在西汉古籍中曾有记载:“曾青得铁则化为铜”,即:曾青(CuSO4)跟铁反应生成铜,试写出该反应的离子方程式 。
(2)在原电池和电解池中,铜常用作电极,下列有关说法正确的是
A.锌铜原电池中铜是正极
B.用电解法精炼铜时粗铜作阴极
C.在镀件上镀铜时铜与电源正极相连
D.铜作阳极时不一定溶解Ⅱ.学习小组对无水硫酸铜分解的产物进行实验探究。
【提出问题】碳酸钙受热分解生成CaO和CO2,那么无水硫酸铜受热分解也只生成CuO和SO3吗?
【设计实验】按如图装置进行试验。
|
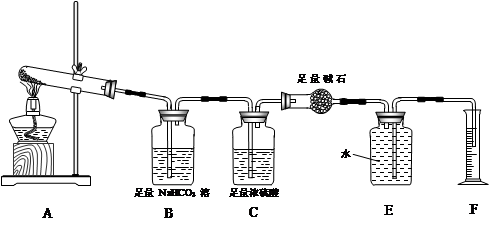 【实验过程】
【实验过程】a.准确称取无水硫酸铜2.40g于装置A试管中加热,直至固体全部变为黑色,经验证该黑色粉末为CuO。
b.实验中,观察到装置E中的水部分被排入量筒中;实验结束后,测得量筒中水的体积为112mL(已折算成标准状态下气体的体积),并测得干燥管D的质量增加了1.32g。
(3)装置C的作用 。
(4)根据装置E、F中现象,推测还有气体 (填分子式)生成;实验生成的SO3为 mol。(5)装置A中反应的化学方程式为 。
【实验结论】无水硫酸铜受热分解不仅仅生成CuO和SO3。
【反思与评价】
(6)任何实验都存在误差,请指出本实验中可能造成误差的因素是 (任写2点)。
Ⅰ(1)Fe+Cu2+== Fe2++Cu (2分)
(2)AC (各1分,共2分,选错不得分)
Ⅱ(3)干燥气体(或吸收混合气体中水蒸气)(2分)
(4)O2(2分) 0.00500(2分)
(5)3CuSO4 3CuO+2SO2↑+SO3↑+O2↑(2分)
3CuO+2SO2↑+SO3↑+O2↑(2分)
(6)①装置内部有气体滞留,气体吸收不完全;②称量造成的误差;③读数造成的误差;④导管中有水残留导致气体体积误差。(2分,答案合理均可给分)
题目分析:Ⅰ(1)铁与硫酸铜发生置换反应,离子方程式为Fe+Cu2+== Fe2++Cu
(2)A、锌铜原电池中锌比铜活泼,作负极,铜是正极,正确;B、用电解法精炼铜时粗铜作阳极,发生氧化反应,阴极有纯铜析出,错误;C、镀铜时铜与电源正极相连,作阳极,发生氧化反应,阴极上有铜析出,达到镀铜目的,正确;D、铜作阳极时一定溶解,错误,答案选AC;
Ⅱ(3)D装置是吸收混合气体,所以C装置是干燥混合气体,防止水进入D中;
(4)根据硫酸铜的元素组成,及该气体不溶于水判断还有O2生成;其物质的量是0.112L/22.4L/mol=0.005mol,所以硫酸铜分解的产物有氧化铜、二氧化硫、三氧化硫、氧气,其化学方程式为3CuSO4 3CuO+2SO2↑+SO3↑+O2↑,由此可知,生成SO3为0.005mol;
3CuO+2SO2↑+SO3↑+O2↑,由此可知,生成SO3为0.005mol;
(5)根据(4)可知装置A中反应的化学方程式为3CuSO4 3CuO+2SO2↑+SO3↑+O2↑
3CuO+2SO2↑+SO3↑+O2↑
(6)本实验中可能造成误差的因素是①装置内部有气体滞留,气体吸收不完全;②称量造成的误差;③读数造成的误差;④导管中有水残留导致气体体积误差。
