现有含CaO杂质的CaC2试样。某研究性学习小组的同学拟用以下三种方案测定CaC2试样的纯度。请填写下列空白:
(1)第一种方案:请从下图中选用适当的装置,设计一个实验,测定CaC2试样的纯度。
所选用装置的连接顺序为(填各接口的字母): 。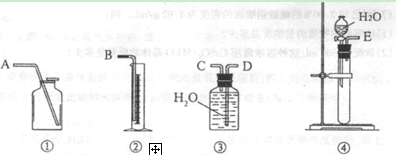
(2)第二种方案:根据试样和水在锥形瓶中反应前后质量的变化,测定CaC2的质量分数。先称取试样1.50g,并称量锥形瓶和水的质量为195.00g,再将试样加入锥形瓶中,反应过程中每隔相同时间测得的数据如下表。
| 读数次数 | 质量/g | |
| 锥形瓶+水+试样 | 第1次 | 196.30 |
| 第2次 | 196.15 | |
| 第3次 | 196.05 | |
| 第4次 | 196.00 | |
| 第5次 | 196.00 |
①计算CaC2的质量分数时,不必作第6次读数的原因是: 。
②此试样中CaC2的质量分数为 。(保留2位有效数字)
(3)第三种方案:称取一定质量的试样(1.60g),操作流程如下:
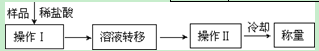
①操作Ⅱ的名称是 。
②在转移溶液时,如溶液转移不完全,则CaC2质量分数的测定结果 (填“偏大”、“偏小”或“不变”)。
⑴E、C、D、 B ⑵锥形瓶内质量已达恒重,82℅;⑶①蒸发结晶,②偏大。
题目分析:⑴该题为通过测量生成的乙炔气体的量来确定CaC2试样的纯度。所以为E C
C D
D B
B
⑵ CaC2+2H2O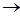 Ca(OH)2+C2H2↑
Ca(OH)2+C2H2↑
64 26
x (195+1.5-196) =0.5g
解之得:x=1.23g
此试样中CaC2的质量分数为: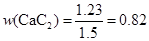
(3)若溶液转移不完全,则测得的气体的质量偏大,所以CaC2质量分数的测定结果偏大。

 CaO+CO2↑
CaO+CO2↑ 2CaSO4
2CaSO4