已知A~I均为中学化学中的常见物质,它们之间的转化关系如图所示,其中A、D为金属单质,反应过程中需要或生成的水及其他部分产物已略去。请回答以下问题:
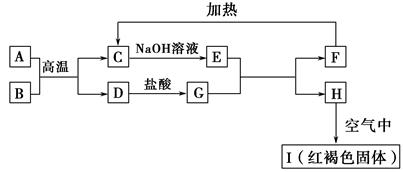
(1)B和F分别是 (填化学式)。
(2)写出下列反应的化学方程式:
①A与B在高温下反应: 。
②H在空气中转变为I: 。
(3)E溶液中所有离子浓度由大到小的顺序是 。
(4)用离子反应方程式表示G溶液呈酸性的原因 ;该反应的平衡常数为 (已知常温下,H的溶度积常数Ksp=8.0×10-16)。
(1)Fe2O3、Al(OH)3
(2)①Fe2O3+2Al 2Fe+Al2O3
2Fe+Al2O3
②4Fe(OH)2+2H2O+O2=4Fe(OH)3
(3)c(Na+)>c([AlCO4]-)>c(OH-)>c(H+)
(4)Fe2++2H2O Fe(OH)2+2H+ 1.25×10-13
Fe(OH)2+2H+ 1.25×10-13
本题以无机框图为载体,考查无机物的性质及化学反应原理,意在考查考生的综合分析能力。(1)根据框中转化关系及题干信息,可以确定I为氢氧化铁。A、D为金属单质,根据A和B的反应条件就可以联想到铝热反应,推测A、D为铝和铁,即A为铝,B为氧化铁,C为氧化铝,D为铁,E为偏铝酸钠,G为氯化亚铁,F为氢氧化铝,H为氢氧化亚铁,I为氢氧化铁。偏铝酸钠水解使溶液呈碱性,所以溶液中离子浓度的大小顺序为c(Na+)>c(AlO2-)>c(OH-)>c(H+);FeCl2溶液中,Fe2+发生水解:Fe2++2H2O Fe(OH)2+2H+,平衡常数K=
Fe(OH)2+2H+,平衡常数K=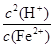 =
=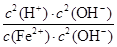 =
=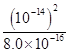 =1.25×10-13。
=1.25×10-13。
