(10分)下图是研究铜与浓硫酸的反应装置:
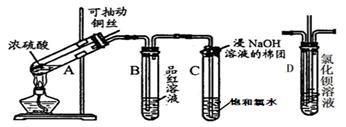
(1)A试管中发生反应的化学方程式为 。
(2)反应一段时间后,可观察到B试管中的现象为 。
(3)C试管口浸有NaOH溶液的棉团作用是 。
(4)实验结束后,证明A试管中反应所得产物是否含有铜离子的操作方法是 。
(5)在铜与浓硫酸反应的过程中,发现有黑色物质出现,经查阅文献获得下列资料。
| 资料1 |  附表铜与浓硫酸反应产生黑色物质的相关性质 |
| 资料2 | X射线晶体分析表明,铜与浓硫酸反应生成的黑色物质为Cu2S、CuS、Cu7S4中的一种或几种。 |
A.铜与浓硫酸反应时所涉及的反应可能不止一个 B.硫酸浓度选择适当,可避免最后产物中出现黑色物质;C.该反应发生的条件之一是硫酸浓度≥15 mol·L D.硫酸浓度越大,黑色物质越快出现、越难消失
(1)Cu+2H2SO4(浓) CuSO4+SO2↑+2H2O ;(2)溶液由红色变成无色
CuSO4+SO2↑+2H2O ;(2)溶液由红色变成无色
(3)吸收Cl2和SO2,防止污染空气;(4)向上拉铜丝,终止反应,冷却后,将A中溶液慢慢倒入盛有少量水的烧杯(试管)里,观察溶液颜色是否为蓝色;(5)A、B、D
题目分析:(1)在A试管中Cu与热的浓硫酸发生反应:Cu+2H2SO4(浓) CuSO4+SO2↑+2H2O ;(2)由于反应产生了SO2气体;该气体由漂白性,能使品红溶液褪色。因此反应一段时间后,可观察到B试管中品红溶液由红色变为无色。(3)Cl2、SO2气体容易导致大气污染,因为SO2和Cl2气体是酸性气体,所以在C试管口用浸有NaOH溶液的棉团来吸收扩散的SO2和 Cl2气体。在C试管中发生反应:Cl2+SO2+2H2O=H2SO4+2HCl。(4)实验结束后,若要证明A试管中反应所得产物含有铜离子,操作方法是向上拉铜丝,终止反应,冷却后,将A中溶液慢慢倒入盛有少量水的烧杯(试管)里,观察溶液颜色是否为蓝色;(5)根据资料提供的信息可知:铜与浓硫酸反应时所涉及的反应可能不止一个;若硫酸浓度选择适当,可避免最后产物中出现黑色物质;硫酸浓度越大,黑色物质越快出现、越难消失。至于硫酸的浓度是多少不容易确定。因此正确选项是A、B、D。
CuSO4+SO2↑+2H2O ;(2)由于反应产生了SO2气体;该气体由漂白性,能使品红溶液褪色。因此反应一段时间后,可观察到B试管中品红溶液由红色变为无色。(3)Cl2、SO2气体容易导致大气污染,因为SO2和Cl2气体是酸性气体,所以在C试管口用浸有NaOH溶液的棉团来吸收扩散的SO2和 Cl2气体。在C试管中发生反应:Cl2+SO2+2H2O=H2SO4+2HCl。(4)实验结束后,若要证明A试管中反应所得产物含有铜离子,操作方法是向上拉铜丝,终止反应,冷却后,将A中溶液慢慢倒入盛有少量水的烧杯(试管)里,观察溶液颜色是否为蓝色;(5)根据资料提供的信息可知:铜与浓硫酸反应时所涉及的反应可能不止一个;若硫酸浓度选择适当,可避免最后产物中出现黑色物质;硫酸浓度越大,黑色物质越快出现、越难消失。至于硫酸的浓度是多少不容易确定。因此正确选项是A、B、D。
