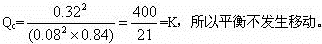在密闭容器中进行的如下反应:2SO2(g)+O2(g)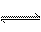 2SO3(g) ,SO2的起始浓度是0.4 mol·L-1,O2的起始浓度是1 mol·L-1。当SO2的转化率为80%时,反应达到平衡状态
2SO3(g) ,SO2的起始浓度是0.4 mol·L-1,O2的起始浓度是1 mol·L-1。当SO2的转化率为80%时,反应达到平衡状态
(1)求反应的平衡常数。
(2)若将平衡时反应混合物的压强增大1倍,平衡将如何移动?
(3)若平衡时反应混合物的压强减小1倍,平衡将如何移动?
(4)平衡时保持体积不变,向平衡混合气体中充入稀有气体Ar,使体系总压变为原来的3倍,平衡又将如何移动?
(1)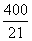 (2)向正反应方向移动 (3)向逆反应方向移动 (4)不移动
(2)向正反应方向移动 (3)向逆反应方向移动 (4)不移动
2SO2(g) + O2(g) 2SO3(g)
2SO3(g)
2 1 2
起始时 0.4 1 0
平衡时 0.4(1-80%) 1-1/2×0.4 0.4×80%
=0.08 ×80% =0.84 =0.32
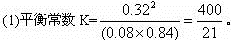

即Qc<K,所以平衡向正反应方向移动。
(3)压强减小1倍,各组分的浓度也减小1倍。
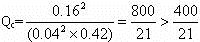
即Qc>K,所以平衡向逆反应方向移动。
(4)保持体积不变,充入稀有气体Ar,尽管总压改变,但反应混合物各组分的浓度保持不变。