以下是分析硫铁矿中FeS2含量的三种方法,各方法的操作流程图如下:
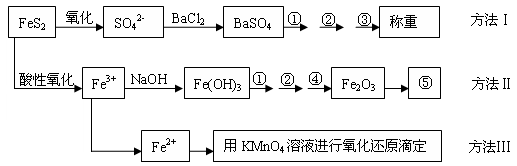
请回答下列问题:
(1)流程图中操作①、②、③分别指的是①_________、②__________、③________。
操作④、⑤用到的主要仪器是:④__________、⑤__________(每空填1-2个仪器)。
(2)判断溶液中SO42-离子已沉淀完全的方法是_________________________________。
(3)某同学用方法Ⅲ测定试样中Fe元素的含量,准确称取一定量的矿石试样,试样经溶解、预处理后,
A.用带有刻度的烧杯配制成100 mL试样溶液。
B.用量筒量取25.00 mL待测溶液,
C.并置于锥形瓶中。
D.用蒸馏水洗涤滴定管后装入KMnO4标准溶液,用该标准溶液滴定待测试样,(E)当溶液变成淡紫红色时,停止滴定,如30秒内不褪色,(F)读取并计算滴定管中消耗的KMnO4标准溶液体积,计算试样中的Fe元素含量。请指出该实验过程中错误操作步骤的编号________________________。(4)某同学采用方法Ⅱ分析矿石中的Fe含量,发现测定结果总是偏高,则产生误差的可能原因是_____________________________________________。
(5)称取矿石试样1.60 g, 按方法Ⅰ分析,称得BaSO4的质量为4.66 g,假设矿石中的硫元素全部来自于FeS2,则该矿石中FeS2的质量分数是___________。
(1)过滤 (1分) 洗涤 (1分) 干燥 (1分) 坩埚、酒精灯 (1分) 天平 (1分)
(2)取上层清液滴加BaCl2溶液,若无白色沉淀生成,说明SO42-沉淀完全 (2分)
(3)A、B、D (3分)
(4)(2分)有三个可能的原因:(写出其中一种,即给2分)
① Fe(OH)3沉淀表面积大,易吸附杂质
②过滤洗涤时未充分将吸附的杂质洗去
③ Fe(OH)3灼烧不充分,未完全转化为Fe2O3
(5)75.0% (3分)
题目分析:(1)从溶液中得到纯净的固体需经过过滤、洗涤、干燥三步,第④步为灼烧使氢氧化铁分解为氧化铁,然后称量氧化铁的质量确定FeS2含量,所以使用的仪器分别为坩埚、酒精灯和天平;(2)取上层清液滴加BaCl2溶液,若无白色沉淀生成,说明SO42-沉淀完全;(3)A、配制溶液要用容量瓶,错误;B、量筒的读数只能精确到十分位,错误;D、滴定管要用待装液润洗,错误。(4)称量的固体质量高,导致结果偏高,故可能的原因有:① Fe(OH)3沉淀表面积大,易吸附杂质 ②过滤洗涤时未充分将吸附的杂质洗去 ③ Fe(OH)3灼烧不充分,未完全转化为Fe2O3;
(5)n(FeS2)=n(SO42-)/2=2n(BaSO4)/2=4.66÷233÷2=0.01mol
该矿石中FeS2的质量分数是0.01×120÷1.60=0.75
