工业上用固体硫酸亚铁制取颜料铁红(Fe2O3),反应原理是:2FeSO4
Fe2O3+SO2↑+SO3↑. △ .
某研究性学习小组用下图所示装置检验该反应所产生的气态物质,然后用装置中A瓶内的混合物来测定已分解的FeSO4的质量.
(SO2沸点为-10.02℃)请回答相关问题:
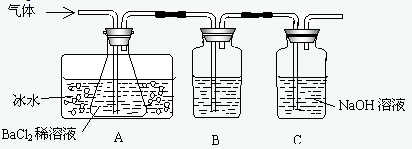
(1)A瓶所盛试剂的作用是______;B瓶所盛的试剂是______;C瓶所盛试剂的作用是______;
(2)A瓶要用冷水冷却的原因是______;
(3)将此反应生成的气体通入A瓶BaCl2溶液中,则______;(填编号)
A.析出BaSO3沉淀 B.析出BaSO4沉淀 C.逸出SO3气体 D.逸出SO2气体
理由是______;
(4)反应后若用A瓶内的混合物来测定已分解的FeSO4的质量,其实验操作的第一步是(简述操作步骤)______.
(1)SO3气体溶于水,发生反应SO3+H2O=H2SO4,H2SO4+BaCl2=BaSO4+2HCl,SO2气体具有漂白性,可使品红溶液褪色,并且SO2有毒,不能排放到空气中,根据SO2气体具有酸性,可用碱液吸收,
故答案为:检验并吸收SO3;品红试液;吸收SO2;
(2)SO3与H2O反应是放热反应,如不冷却,通入品红中的气体中含有SO3气体,故答案为:SO3与H2O反应放出大量的热;
(3)SO2、SO3的混合气体溶于水,发生反应SO3+H2O=H2SO4,同时放出大量的热,使SO2的溶解度减少而逸出SO2气体,又由H2SO4与BaCl2反应析出BaSO4沉淀,在酸性溶液中不可能产生BaSO3沉淀,将此反应生成的气体通入A瓶BaCl2溶液中,会有BaSO4沉淀生成,并析出SO2气体,
故答案为:B、D; SO2、SO3的混合气体溶于水,发生反应SO3+H2O=H2SO4,同时放出大量的热,使SO2的溶解度减少而逸出SO2气体,又由H2SO4与BaCl2反应析出BaSO4沉淀,在酸性溶液中不可能产生BaSO3沉淀;
(4)测定已分解的FeSO4的质量,应使SO3气体完全生成BaSO3沉淀,否则会有较大误差,故答案为:A瓶中滴入BaCl2溶液,直至不再产生新的沉淀.
