碳酸氢铵是我国主要的氮肥品种之一,在贮存和运输过程中容易挥发损失。为了鉴定其质量和确定田间施用量,必须测定其含氮量。
Ⅰ.某学生设计了一套以测定二氧化碳含量间接测定含氮量的方法。将样品放入圆底烧瓶中:
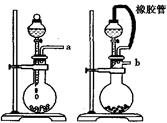
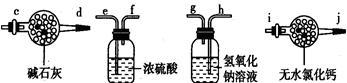
(1)请选择必要地装置,按气流方向连接顺序为 。
(2)分液漏斗中的液体最适合的是 。
A.稀盐酸
B.稀硫酸
C.浓硝酸
D.氢氧化钠(3)连在最后的装置起到的作用 。
Ⅱ.如果氮肥中成分是(NH4)2SO4,则可以用甲醛法测定含氮量。甲醛法是基于甲醛与一定量的铵盐作用,生成相当量的酸,反应为2(NH4)2SO4+6HCHO→(CH2)6N4 +2H2SO4 + 6H2O,生成的酸再用氢氧化钠标准溶液滴定,从而测定氮的含量。步骤如下:
(1)用差量法称取固体(NH4)2SO4样品0.6g于烧杯中,加入约30mL蒸馏水溶解,最终配成100mL溶液。用 (填“酸式”或“碱式”)滴定管准确取出20.00mL的溶液于锥形瓶中,加入18%中性甲醛溶液5mL,放置5min后,加入1~2滴 指示剂(已知滴定终点的pH约为8.8),用浓度为0.08mol/L氢氧化钠标准溶液滴定,读数如下表:
| 滴定次数 | 滴定前读数(mL) | 滴定后读数(mL) |
| 1 | 1.20 | 16.21 |
| 2 | 3.00 | 18.90 |
| 3 | 4.50 | 19.49 |
达滴定终点时的现象为 ,由此可计算出该样品中的氮的质量分数为 。
(2)在滴定实验结束后发现滴定用的碱式滴定管玻璃尖嘴内出现了气泡,滴定开始时无气泡,则此实验测定的含氮量比实际值 (填“偏大”“偏小”或“无影响”)。
Ⅲ.如果测定碳酸氢铵中的含氮量时,使用甲醛法是否合理 (填“是”或“否”),理由是 。
Ⅰ(1)b-e,f-h,g-c (2)B (3)防止空气中水和二氧化碳进入装置影响实验结果;
Ⅱ(1)酸式 酚酞 溶液从无色变为浅红色 ,30s内不褪色 14% (2)偏小
Ⅲ否,因为用氢氧化钠标准溶液滴定时,溶液中HCO3—中的H+也会和氢氧化钠中和
题目分析:Ⅰ.(1)本题考查实验装置的选择和连接,实验装置的连接顺序为发生装置、净化装置、干燥装置、性质或收集装置、尾气处理装置。一般除杂在前,干燥在后;若是燃烧管除杂,则干燥在前;若用洗气瓶,则“长进短出”,若用干燥管,则“大进小出”;根据题意知,装有氢氧化钠溶液的洗气瓶为二氧化碳的吸收装置,为保证实验结果准确,必须防止水蒸气和外界空气的干扰;为保证分液漏斗内液体顺利流下,应选第二个装置作为二氧化碳的发生装置;根据上述分析连接次序为:b-e,f-h,g-c;(2)盐酸和硝酸易挥发,会干扰二氧化碳的测定,氢氧化钠溶液与样品反应不会生成二氧化碳,所以分液漏斗内的液体应为稀硫酸,选B;(3)连在最后的装置起到的作用为防止空气中水和二氧化碳进入装置影响实验结果;
Ⅱ(1)(NH4)2SO4属于强酸弱碱盐,水解显酸性,所以用酸式滴定管准确取出20.00mL的溶液;滴定终点的pH约为8.8,酚酞变色范围为8.2——10,应用酚酞作指示剂;用浓度为0.08mol/L氢氧化钠标准溶液滴定,达滴定终点时的现象为溶液从无色变为浅红色 ,且30s内不褪色;分析题给数据知,第二组数据误差较大,应舍弃,所用氢氧化钠溶液的体积为15.00mL 根据题给反应得氮原子与氢氧化钠之间的关系式:N——NaOH,代入数据计算可得,0.6g样品中含氮原子的物质的量为0.08mol/L×0.015L×5=0.006mol,其质量为0.084g,质量分数为14%;(2)在滴定实验结束后发现滴定用的碱式滴定管玻璃尖嘴内出现了气泡,滴定开始时无气泡,代入计算得氢氧化钠溶液的体积偏小,则此实验测定的含氮量比实际值偏小;
Ⅲ.如果测定碳酸氢铵中的含氮量时,使用甲醛法不合理,理由是因为用氢氧化钠标准溶液滴定时,溶液中HCO3—中的H+也会和氢氧化钠中和。