某兴趣小组去一家回收含铜电缆废料的工厂做社会调查,技术人员向他们展示两个方案,并提出下列问题:
方案甲:
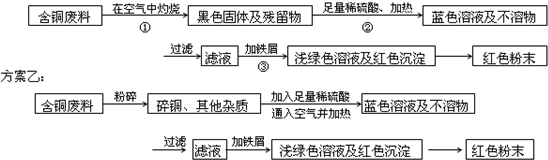
方案乙:
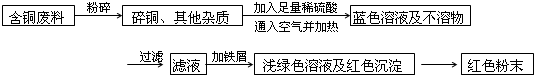
(1)两个方案哪个符合当前的绿色理念:______;
(2)写出方案甲中步骤②、③反应的离子方程式:______、______;
(3)无论是甲还是乙方案,在“加铁屑”时,都加入稍过量的铁屑,你认为这么做的道理是:______;
(4)①用简便的方法检验红色粉末中含有过量的铁屑:______;②如何除去红色粉末中所含过量的Fe得干燥的红色粉末:______.
(1)方案乙中所有的铜原子均转化为硫酸铜,操作简单,符合当前的绿色理念,故答案为:乙;
(2)②氧化铜属于碱性氧化物,能和硫酸反应生成盐和水,方程式为CuO+2H+=Cu2++H2O; ③铁排在金属铜的前面,能将铜从其盐中置换出来,方程式为Fe+Cu2+=Fe2++Cu;
故答案为:CuO+2H+=Cu2++H2O;Fe+Cu2+=Fe2++Cu;
(3)加入足量的铁,能使所有的金属铜均被置换出来,故答案为:确保Cu完全置换出来;
(4)①铁可以被磁铁吸引,也可以和强酸反应产生氢气,可用磁铁检验是否含铁屑(或取样品加入盐酸看有没有气泡产生); ②铁能溶于盐酸或硫酸而铜不溶,要除去红色粉末铜中所含过量的Fe得干燥的铜,可以将所得铜粉用稀盐酸或稀硫酸清洗后再洗涤、干燥,故答案为:用磁铁检验是否含铁屑(或取样品加入盐酸看有没有气泡产生);将所得铜粉用稀盐酸或稀硫酸清洗后再洗涤、干燥.
