问题
填空题
(12分)工业上用CO生产燃料甲醇。一定条件下发生反应:CO(g)+2H2(g)
CH3OH(g)。图1表示反应进行过程中能量的变化(曲线a未使用催化剂,曲线b使用催化剂),图2表示一定温度下,在体积为2L的密闭容器中加入4mol H2和一定量的CO后,CO和CH3OH(g)的浓度随时间变化情况。
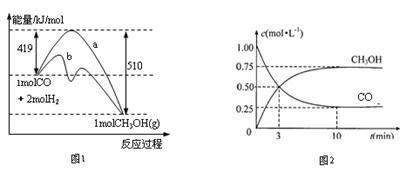
(1)下列说法正确的是______________
A.反应进行到3min时达到化学平衡状态
B.是否使用催化剂对反应前后的能量变化没有影响
C.当反应物消耗量一定时,若反应生成液态甲醇,能量变化值会更大
D.平衡时氢气的浓度为1mol/L(2)从反应开始到平衡状态,用CO浓度变化表示的反应速率为_______________,H2的转化率为______________。
(3)当有0.25mol CH3OH生成时会__________(填吸收或放出)___________kJ的热量。
答案
(1)BC(4分,每个2分,多选倒扣)
(2)0.075mol/(Ls); 75%(每空2分)
(3)放出; 22.75(每空2分)
