问题
实验题
(7分)某同学在自主学习酸的知识时,设计了以下实验报告,请将实验报告补充完整。
【实验目的】
【实验用品】试管、铁片、铜片、稀盐酸、稀硫酸、NaOH溶液、石蕊和酚酞试液等
【实验内容】
| 实验 步骤 | ①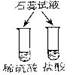 | ②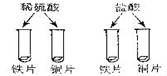 | ③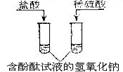 |
| 实验 现象 | 溶液变为 色 | 稀酸中的铁片表面都有 产生; 铜片表面都没有明显现象 | 溶液由红色变为无色 |
| 分析 与 结论 | 结论: 稀酸能与指示剂作用 | 铁与稀硫酸反应的化学方程式为
结论:稀酸能与较活泼金属反应 | 结论: 酸能 |
答案
(7分)探究(或认识)稀酸的通性 红 气泡
方程式Fe+H2SO4═FeSO4+H2↑ 酸能与碱反应
酸的溶液中都能电离出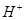
(实验目的)可根据该实验的内容及其结论逆向推导为:探究稀酸的通性.
(实验内容):根据实验步骤的内容依次判断,步骤①:石蕊试液分别滴入稀硫酸、盐酸中,溶液都变为红色;步骤②:铁在金属活动性顺序中排在H的前面,铁能置换稀硫酸或盐酸里的氢,反应时铁片表面都有氢气的气泡产生,铁与稀硫酸反应生成硫酸亚铁和氢气;步骤③:在含有酚酞试液的氢氧化钠溶液中分别滴入盐酸和稀硫酸,溶液由红色变为无色,说明酸能与碱反应.
(实验思考):从物质组成的角度解释稀酸具有酸的通性的原因是酸都含有氢元素.
故答案:(实验目的):探究(或认识)稀酸的通性.
(实验内容):
| 实验步骤 | |||
| 实验现象 | 红 | 气泡 | |
| 分析与结论 | Fe+H2SO4═FeSO4+H2↑ | 酸能和碱反应 |