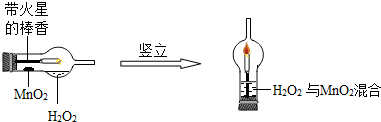
实验创新是中学生最为重要的科学素养.下图是某学校师生对“MnO2催化H2O2分解实验装置的创新设计”,实验过程如下:
①将一支球形干燥管水平放置,用滴管吸取3ml(密度为lg/ml)质量分数为5%的H2O2加入干燥管的球泡内,再用药匙取0.2gMnO2粉末,加在干燥的进气管的管壁上.
②点燃橡胶塞上固定的棒香后,塞紧干燥管并将其竖立,观察现象.
请分析回答:(1)可观察带到火星的棒香立即______.
(2)写出上述实验中H2O2分解的化学反应方程式______.
(3)假定上述实验中的H2O2完全反应,可产生氧气的质量为______g.(精确到0.01)
(4)下列各项是同学们对该创新实验的评价,你认为评价不合理的是______.(填序号)
A、实验中所用的仪器、材料及药品均易得到
B、实验使用的药品用量太大
C、反应速度太慢,耽误时间
D、实验现象明显,整个装置好似点燃的灯塔,趣味性强
(1)过氧化氢溶液在二氧化锰的催化作用下能快速放出氧气,因为氧气具有支持燃烧的性质,所以能使带到火星的棒香立即复燃,故答案为:复燃;
(2)注意书写化学方程式的步骤,明确反应物、生成物、反应条件,故答案为:2H2O2
2H2O+O2↑ MnO2 .
2H2O2H2O+O2↑;
(3)根据化学方程式计算的步骤,由过氧化氢的质量去求算产生氧气的质量,
设H2O2完全反应,可产生氧气的质量为x,
H2O2的质量为:3ml×lg/ml×5%=0.15g
2H2O2
2H2O+O2↑ MnO2 .
68 32
0.15g x
=68 32 0.15g x
68 32
解得:x=0.07g
故答案为:0.07
(4)评价要实事求是,不能随便乱说,实验使用的药品用量不算大;反应速度不慢,故答案为:BC
