下列两个反应均为在溶液中进行的反应,试按下列要求作答:
①用双线桥标明下列反应中电子的转移及数目;
②在表格中填出反应式中的氧化剂、还原剂,氧化产物、还原产物.
③将其改写成离子方程式;
(1)2FeCl3+H2S═2FeCl2+S↓+2HCl
| 氧化剂: | 还原剂: | ||
| 氧化产物: | 还原产物: |
(2)MnO2+4HCl(浓)
MnCl2+2H2O+Cl2↑△ .
| 氧化剂: | 还原剂: | ||
| 氧化产物: | 还原产物: |
(1)反应2FeCl3+H2S═2FeCl2+S↓+2HCl中,Fe元素的化合价由+3价降低为+2价,得电子数为2×e-,S元素的化合价由-2价升高到0,
失去电子数为2e-,用双线桥标明下列反应中电子的转移及数目为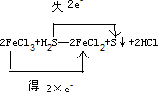 ,
,
该反应中的氧化剂为FeCl3,还原剂为H2S,氧化产物为S,还原产物为FeCl2,
该反应改为离子反应时,H2S、S应保留化学式,则离子方程式为2Fe3++H2S=2Fe2++S↓+2H+,
故答案为: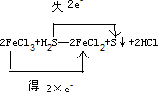 ;FeCl3;H2S;S;FeCl2;2Fe3++H2S=2Fe2++S↓+2H+;
;FeCl3;H2S;S;FeCl2;2Fe3++H2S=2Fe2++S↓+2H+;
(2)反应MnO2+4HCl(浓)
MnCl2+2H2O+Cl2↑中,Mn元素的化合价由+4价降低为+2价,MnO2为氧化剂,得2e-,Cl元素由-1价升高到0,HCl为还原剂,失2×e-,△ .
用双线桥标明下列反应中电子的转移及数目为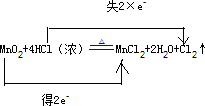 ,
,
氧化剂被还原,则还原产物为MnCl2,还原剂被氧化,则氧化产物为Cl2,
该反应改为离子反应时,MnO2、Cl2、H2O应保留化学式,则离子反应为MnO2+4H++2Cl-
Mn2++Cl2↑+2H2O,△ .
故答案为: ;MnO2;HCl;Cl2;MnCl2;MnO2+4H++2Cl-
;MnO2;HCl;Cl2;MnCl2;MnO2+4H++2Cl-
Mn2++Cl2↑+2H2O.△ .
