某实验小组欲制取氧化铜,并证明氧化铜能加快氯酸钾的分解,进行如下实验:
Ⅰ.制取氧化铜
①称取2gCuSO4•5H2O研细后倒入烧杯,加10mL蒸馏水溶解;
②向上述CuSO4溶液中逐滴加入NaOH溶液,直到不不规则产生沉淀,然后将所得混合物转移到蒸发皿,加热至沉淀传问变为黑色;
③将步骤②所得混合物过滤、洗涤,晾干后研细备用.
回答下列问题:
(1)上述实验①、③步骤中需要使用玻璃棒的是______(填实验步骤序号).
(2)步骤、中研磨固体所用仪器的名称是______.
Ⅱ.证明氧化铜能加快氯酸钾的分解,并与二氧化锰的催化效果进行比较用如图装置进行实验,实验时均以生成25mL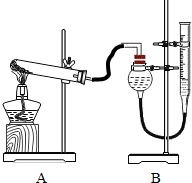 气体为准,其它可能影响实验的因素均已忽略.相关数据见下表:
气体为准,其它可能影响实验的因素均已忽略.相关数据见下表:
| 实验序号 | KClO3质量 | 其它物质质量 | 待测数据 |
| ④ | 1.2g | 无其他物质 | |
| ⑤ | 1.2g | 0.5gCuO | |
| ⑥ | 1.2g | 0.5gMnO2 |
(4)为探究CuO在实验⑤中是否起催化作用,需补做以下实验(无需写出具体操作):
a.______;
b.检验CuO的化学性质是否改变.
c.查阅资料后了解,MnO2对KClO3的催化过程由以下三个反应组成,请将第二个反应补充完整.
a.KClO3+2MnO2=2KMnO4+Cl2+O2↑
b.2KMnO4→K2MnO4+______
c.K2MnO4+Cl2=2KCl+MnO2+O2↑
(1)①溶解过程中用玻璃棒搅拌,加快溶解速度;②中用玻璃棒转移固体;③中用玻璃棒引流液体;
(2)研磨固体在研钵中进行;
(3)证明氧化铜能加快氯酸钾的分解,并与二氧化锰的催化效果进行比较,对比实验一定要控制变量,此实验中应控制氯酸钾质量、气体的体积、氧化铜与二氧化锰的质量相等,可变的量是生成等体积(25mL)气体所需用的时间.
(4)催化剂是能改变化学反应速度,而本身质量和化学性质不变,故还应检验氧化铜的质量是否改变;
高锰酸钾分解生成锰酸钾、二氧化锰和氧气,
故答案为:(1)①②③(2)研钵;(3)时间;(4)检验氧化铜质量是否改变;(5)2KMnO4
K2MnO4+MnO2+O2↑△ .
