(7分)一定温度下,物质的量浓度分别为2mol/L和1.5mol/L的SO2(g)和O2(g)在密闭容器中发生反应:2SO2(g)+ O2(g) 2SO3(g),4min后反应达到平衡状态,测得容器中SO2(g)的转化率为60%,试求,在该温度下:
2SO3(g),4min后反应达到平衡状态,测得容器中SO2(g)的转化率为60%,试求,在该温度下:
(1)用SO2表示的平均反应速率;
(2)平衡时O2的转化率;
(3)此反应的平衡常数。
(共7分)由题可知,SO2的变化浓度为2mol·L-1×60%=1.2mol·L-1,则O2和SO3的变化浓度分别为0.6mol·L-1和1.2mol·L-1,则:
2SO2(g) + O2(g)  2SO3(g)
2SO3(g)
起始时各物质浓度/mol·L-1 2 1.5 0
各物质变化浓度/mol·L-1 1.2 0.6 1.2
平衡时各物质浓度/mol·L-1 0.8 0.9 1.2 (1分)
(1)v(SO2)=1.2mol·L-1÷4min=0.3 mol·L-1·min-1  (2分)
(2分)
(2)O2的转化率为0.6mol·L-1÷1.5mol·L-1×100%="40% " (2分)
(3)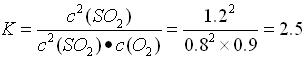 (2分)
(2分)
