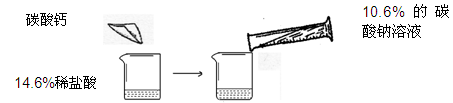
某同学做了如下图所示的实验,在14.6%的稀盐酸中加入碳酸钙,后加入10.6%的碳酸钠溶液
| 第一次 | 第二次 | |
| 14.6%的稀盐酸的质量 | m | m |
| 加入碳酸钙的质量 | 10g | 20g |
| 加入10.6%的碳酸钠溶液的质量 | 100g | 200g |
| 加入碳酸钠溶液后,实验现象 | 只有气泡 | 只有白色沉淀 |
写出实验一中发生化学反应的方程式
第一次实验中加入碳酸钙后溶液中溶质成分
根据已知条件列出求解第二次实验生成沉淀的质量的比例式
实验中加入稀盐酸m的质量为
若将第二次反应后的溶液蒸发191.2g水,则所得不饱和溶液中溶质的质量分数为
若用溶质质量分数29.2%的浓盐酸配置实验所需的稀盐酸,则需要加水的质量
(1)CaCO3+2HCl==CaCl2+H2O+CO2↑和Na2CO3+2HCl==2NaCl+H2O+CO2↑
(2)氯化钙、氯化氢 (3)106:100=21.2g:X
(4)100g (5)23.4% (6)100g
题目分析:(1)实验一在加入碳酸钠溶液后,只有气泡产生,说明盐酸过量,所以发生反应的化学方程式:CaCO3+2HCl==CaCl2+H2O+CO2↑和Na2CO3+2HCl==2NaCl+H2O+CO2↑
(2)根据上面的分析,盐酸过量,加上生成的氯化钙,所以第一次实验中加入碳酸钙后溶液中溶质成分:氯化钙、氯化氢
(3)根据实验一的数据,可以判断20g的碳酸钙与稀盐酸恰好完全反应,故生成的白色沉淀全部是氯化钙与加入的碳酸钠溶液反应生成的碳酸钙,方程式为:CaCl2+Na2CO3==CaCO3↓+2NaCl,根据Na2CO3与CaCO3的质量关系为106:100,而碳酸钠的质量=200g×10.6%=21.2g,所以第二次实验生成沉淀的质量的比例式:106:100=21.2g:X
(4)根据分析,加入20g的碳酸钙恰好能与稀盐酸反应,所以根据方程式:CaCO3+2HCl==CaCl2+H2O+CO2↑中CaCO3与HCl的质量关系为100:73,
解:CaCO3+2HCl==CaCl2+H2O+CO2↑
100 73
20g 14.6%×m
100:73=20g:14.6%×m
m=100g
(5)根据第(3)问分析,20g的碳酸钙与稀盐酸恰好完全反应:CaCO3+2HCl==CaCl2+H2O+CO2↑,根据CaCO3与CO2的质量关系100:44,可计算出产生二氧化碳的质量为8.8g,而生成的白色沉淀全部是氯化钙与加入的碳酸钠溶液反应生成的碳酸钙,方程式为:CaCl2+Na2CO3==CaCO3↓+2NaCl,根据Na2CO3与CaCO3、NaCl的质量关系,分别计算出CaCO3、NaCl的质量
解:设CaCO3、NaCl的质量分别为x、y
CaCl2+Na2CO3==CaCO3↓+2NaCl
106 100 117
200g×10.6% x y
106 : 100="200g×10.6%" :x
x=20g
106 : 117="200g×10.6%" :y
y=23.4g
所以反应后溶液质量=100g+20g-8.8g+200g-20g=291.2g
故将第二次反应后的溶液蒸发191.2g水,则所得不饱和溶液中溶质的质量分数=23.4g/291.2g-191.2g×100%=23.4%
(6)因为两次实验总共消耗盐酸溶液质量为200g,根据溶液稀释过程中,溶质的质量不变,可设需要浓盐酸的质量为a,可列式为:a×29.2%=200×14.6%,所以a=100g,所以需要加水的质量=200g-100g=100g
