生产着色铝片的工艺流程如下:
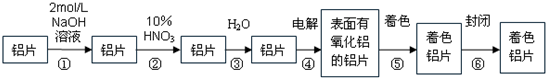
请回答下列问题:
(1)第①步中NaOH溶液的作用是______.
(2)第②步HNO3的作用是对铝片进行抛光,写出其反应的离子方程式______.
(3)在第④步电解是以铝为阴极,铝片为阳极,在硫酸介质中控制电压电流,使阳极放出O2与Al反应使铝表面形成一层致密的氧化膜.写出有关的电极反应式:阴极:______,阳极:______.
(4)氧化膜质量的检验:取出铝片干燥,在氧化膜未经处理的铝片上分别滴一滴氧化膜质量检查液(3gK2CrO4+75mL水+25mL浓盐酸),判断氧化膜质量的依据是______.
A.铝片表面有无光滑 B.比较颜色变化
C.比较质量大小 D.比较反应速率大小
(5)将已着色的铝干燥后在水蒸气中进行封闭处理约20~30min,封闭的目的是使着色的氧化膜更加致密,有关反应化学方程式是______.
(1)因铝表面的油污,用热碱液除可以金属表面油污,故答案为:洗去铝表面的油污;
(2)因铝与硝酸反应:Al+4HNO3=Al(NO3)3+NO↑+2H2O,离子方程式为:Al+4H++NO3-=Al3++NO↑+2H2O,故答案为:Al+4H++NO3-=Al3++NO↑+2H2O;
(3)阴极是溶液中的阳离子H+得到电子:6H++6e-=H2↑;阳极是水中的氢氧根离子放电产生氧气,放出O2与Al反应使铝表面形成一层致密的氧化膜:2Al+3H2O-6e-=Al2O3+6H+,故答案为:6H++6e-=H2↑;2Al+3H2O-6e-=Al2O3+6H+;
(4)因K2CrO4是黄色的,其中的Cr(+6价)有氧化性能和Al反应应该是被还原成+3价(绿色),颜色发生了变化,故选:B.
(5)因Al和H2O(g)生成了氧化铝,所以化学方程式为:2Al+3H2O(g)
Al2O3+3H2(g),故答案为:2Al+3H2O(g) △ .
Al2O3+3H2(g). △ .
