某中学有甲、乙两个探究性学习小组,他们拟用小颗粒的铝铜合金与足量的稀硫酸反应测定通常状况(约20℃、1.01×105Pa)下的气体摩尔体积(Vm).
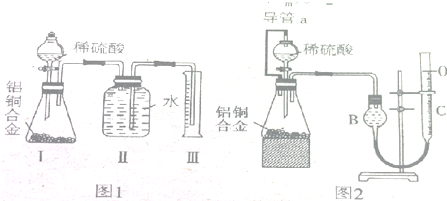
(一)甲组同学拟设计如图1所示的装置来完成实验.
(1)写出装置I中发生反应的离子方程式:______.
(2)实验开始时,先打开分液漏斗上口的玻璃塞,再轻轻旋开其活塞,一会儿后发现稀硫酸不能顺利滴入锥形瓶中.请帮助他们分析其原因:______.
(3)实验结束时,生成氢气的体积近似等于:______.
(4)锥形瓶中残存的氢气对实验结果是否有影响:______(填“有”、“没有”、或“不能判断”),简述理由:______.
(二)乙组同学仔细分析了甲组同学的实验装置后以为,稀硫酸滴入锥形瓶中,即使不生成氢气,也会将瓶中的空气排出,使所测氢气的体积偏大;实验结束后,连接广口瓶
和量筒的导管中有少量水存在,使所测氢气的体积偏小.于是他们设计了如图2所示的实验装置.
(1)装置中导管a的作用是:______.
(2)实验中准确测定出4个数据,如下表:
| 实验前 | 实验后 | |
| 铝铜合金质量(g) | m1 | m2 |
| 量液管(C)体积(mL) | V1 | V2 |
(一)
(1)铝和稀硫酸反应生成硫酸铝和氢气,其离子方程式为:2Al+6H+=2Al3++3H2↑.
故答案为:2Al+6H+=2Al3++3H2↑.
(2)铝与稀硫酸反应产生的氢气使锥形瓶内气压增大,锥形瓶内的压强大于大气压,所以稀硫酸不能顺利滴入锥形瓶中.
故答案为:铝与稀硫酸反应产生的氢气使锥形瓶内气压增大.
(3)气体产生的压强导致水从集气瓶中排出,且氢气不易溶于水,所以收集到的水的体积近似等于氢气的体积.
故答案为:收集到水的体积近似等于氢气的体积.
(4)装置中有空气存在,生成的氢气不溶于水,在相同温度和压强下,参与氢气的体积与排出空气的体积相等,
所以没有影响.
故答案为:没有、相同温度和压强下,参与氢气的体积与排出空气的体积相等
(二)
(1)铝与稀硫酸反应产生的氢气使锥形瓶内气压增大,锥形瓶内的压强大于大气压,导管a使锥形瓶内的气体进入分液漏斗上方,使分液漏斗上方的压强增大,稀硫酸顺利滴下.
故答案为:平衡锥形瓶与分液漏斗内的压强,使稀硫酸顺利滴下.
(2)2Al+6H+=2Al3++3H2↑.
2mol 3mol
mol m1-m2 27
mol(V2-V1)×10-3 Vm
Vm=
L/mol9(V2-v1) 500(m1-m2)
故答案为:
L/mol9(V2-V1) 500(m1-m2)
