(共16分)如下图,甲、乙、丙分别表示在不同条件下可逆反应:A(g)+B(g)  xC(g)的生成物 C在反应混合物中的百分含量(C%)和反应时间(t)的关系。
xC(g)的生成物 C在反应混合物中的百分含量(C%)和反应时间(t)的关系。
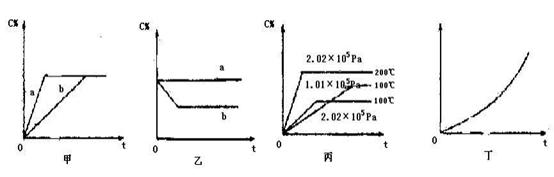
(1)若甲图中两条曲线分别代表有催化剂和无催化剂的情况,则 曲线表示无催化剂时的情况,速率:a b(填:大于、小于或等于)
(2)若乙图表示反应达到平衡后,分别在恒温恒压条件下和恒温恒容条件下向平衡混合气体中充入He气后的情况,则 曲线表示恒温恒容的情况,此时该恒温恒容中
C% (填:变大、变小或不变)
(3)根据丙图可以判断该可逆反应的正反应是 热反应(填:放热、吸热),计量数x的值是 ;
(4)丁图表示在某固定容器的密闭容器中,上述可逆反应达到平衡后,某物理量随着温度(T)的变化情况,根据你的理解,丁图的纵坐标可以是 ,[填:①C% ②A的转化率 ③B的转化率④压强⑤c(A)⑥c(B)];升温平衡移动的方向为 。(填:左移或右移)
(1)b 大于 (2)a 不变 (3)吸 大于2(或大于等于3)
(4)①②③④ 右
(1)对于某可逆反应来说,加入催化剂,仅仅是加快反应速率,不影响平衡的移动,所以b曲线表示无催化剂,速率大小为:a大于b;
(2)恒温恒容条件下,加入无关气体氦气,平衡不移动,则曲线a 为恒温恒容,C%不变。
(3)在相同的压强下,温度越高C%的含量越高,即可知该反应的正反应为吸热反应;在相同温度下,压强越大,C%的含量越小,即可知该反应的正反应方向为气体体积增大的反应,x的值大于2(或大于等于3)。
(4)根据图示可知,①②③④符合题意;由于该反应的正反应为吸热反应,升温平衡向右移动。
