(12分) 恒容密闭容器中,某化学反应2A  B+D在四种不同条件下进行,B、D起始浓度为0,反应物A的浓度(mol/L)随反应时间(min)的变化情况如下表:
B+D在四种不同条件下进行,B、D起始浓度为0,反应物A的浓度(mol/L)随反应时间(min)的变化情况如下表:
| 实验序号 | 浓度(mol/L) | 时间(min) | |||||||
| 0 | 10 | 20 | 30 | 40 | 50 | 60 | |||
| 1 | 温 度 | 8000C | 1.0 | 0.80 | O.64 | 0.57 | 0.50 | 0.50 | 0.50 |
| 2 | 8000C | C2 | 0.60 | 0.50 | 0.50 | 0.50 | 0.50 | 0.50 | |
| 3 | 8000C | C3 | 0.92 | 0.75 | 0.63 | 0.60 | 0.60 | 0.60 | |
| 4 | 8200C | 1.0 | 0.40 | 0.25 | 0.20 | 0.20 | 0.20 | 0.20 | |
(1)在实验1,反应在前20min内用B的浓度变化来表示的平均速率
为 mol/(L·min)。
(2)在实验2,A的初始浓度c2= mol/L,反应在 20分钟内就达到
平衡,可推测实验2中还隐含的条件是 。
(3)设实验3的反应速率为υ3,实验1的反应速率为υ1(用同种物质的浓度变
化表示),则达到平衡时υ3 υ1(填>、=、<=)
且c3 = mol/L。
(4)比较实验4和实验1,可推测该反应是 反应(选填“吸热”、“放热”)。
(5) 800℃时,反应2A  B+D的平衡常数= ,
B+D的平衡常数= ,
实验2中达到平衡时A的转化率= 。
(12分)(1)0.009 (2分) (2)1.0(1分) 使用了催化剂(1分)
(3) >(1分) 1.2 (2分)
(4) 吸热(1分) (5) 0.25(2分) 50%(2分)
(1)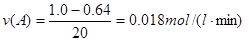 ;
;
则
(2)由于实验2平衡时A的浓度与实验1相同,互为等效平衡,即实验2,A的初始浓度c2=1.0 mol/L,实验2在平衡时时间更短,说明使用了催化剂;
(3)实验3中平衡时A的浓度更高,则说明实验3的起始浓度更高,化学反应速率更快;根据温度不变平衡常数不变可求得c3 =" 1.2" mol/L。
(4)由表中数据可得,随温度的升高A的浓度减少,即平衡向正反应方向移动,所以正反应方向为吸热反应;
(5)800℃时,反应2A  B+D的平衡常数= 0.25;实验2中达到平衡时A的转化率=50%
B+D的平衡常数= 0.25;实验2中达到平衡时A的转化率=50%
