合成氨尿素工业生产过程中涉及到的物质转化过程如下图所示。
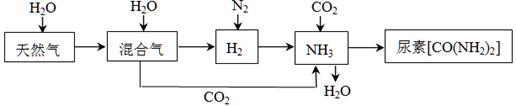
(1)天然气(主要成分为CH4)在高温、催化剂作用下与水蒸气反应生成H2和CO的化学方程式为 。
(2)甲烷是一种清洁燃料,但不完全燃烧时热效率降低,同时产生有毒气体造成污染。
已知:CH4(g) + 2O2(g)=CO2(g) + 2H2O(l) ΔH1=―890.3 kJ/mol
2CO (g) + O2(g)=2CO2(g) ΔH2=―566.0 kJ/mol
则甲烷不完全燃烧生成一氧化碳和液态水时的热效率是完全燃烧时的_____倍(计算结果保留1位小数)。
(3)甲烷燃料电池可以提升能量利用率。下图是利用甲烷燃料电池电解50 mL 2 mol·L-1的氯化铜溶液的装置示意图:
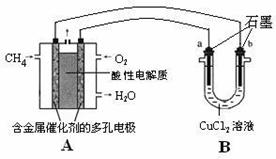
请回答:
①甲烷燃料电池的正极反应式是____ ____。
②当线路中有0.1 mol电子通过时,________(填“a”或“b”)极增重________g。
(4)运输氨时,不能使用铜及其合金制造的管道阀门。因为在潮湿的环境中,金属铜在有NH3存在时能被空气中的O2氧化,生成[Cu(NH3)4]2+,该反应的离子方程式为 。
(10分)
(1)CH4 + H2O  CO + 3H2(2分)
CO + 3H2(2分)
(2)0.7(2分)
(3)① O2+4 H++4e-==2H2O (2分) ② b (1分) 3.2(1分)
(4)2Cu + 8NH3 + O2 + 2H2O ="==" 2[Cu(NH3)4]2+ + 4OH-(2分)
题目分析:(1)根据题中提供的反应物、生成物和条件可以书写方程式,方程式为CH4 + H2O  CO + 3H2。
CO + 3H2。
(2)(由第一个式子乘以2在减去第二个式子)再除以2得:CH4(g) + 3/2O2(g)=CO (g) + 2H2O(l) ΔH=- 607.3 kJ/mol。(607.3 kJ/mol)/ (890.3 kJ/mol)=0.7。
(3)①充入O2的一极是正极,失去电子,反应式是O2+4H++4e-==2H2O。
②Cu2++2e-=Cu,0.1mol电子,得铜为3.2g。b极是阴极得电子,故b及质量增加。
(4)根据题中给提供的反应物和生成物书写,离子方程式为:2Cu + 8NH3 + O2 + 2H2O ="==" 2[Cu(NH3)4]2+ + 4OH-。
点评:本题考查的是化学计算、合成氨、燃料电池和电解原理等知识,题目难度中,对各个知识点原理都清楚才能解答此题。
