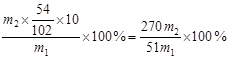(16分)某研究小组取足量形状、质量均相同的铝片,分别与浓度均为6 mol•L-1的等体积的盐酸、氢氧化钠溶液充分反应后,取出剩余的铝片洗净、干燥、称量。
(1)上述反应剩余铝片的质量,前者________后者(填“大于”或“小于”或“等于”)。
(2)观察铝片与盐酸反应后的溶液较浑浊,且试管底部有少量黑色固体。
查资料已知:
①铝与盐酸反应,因反应过快而变成粉末分散到溶液中,形成黑色固体
②电解法冶炼铝所用的原料氧化铝是从铝土矿中提取的,氧化铝中往往还含有微量的氧化铁和二氧化硅杂质。写出在电解池中生成的铝与杂质二氧化硅反应的化学方程式: ________。
(3)为探究(2)中黑色固体的成分,提出合理假设。
假设1:黑色固体是Al和Fe
假设2:黑色固体是Al和Si
假设3:黑色固体是Al和_______________
(4)设计实验方案,基于假设3进行实验,验证黑色固体含有Al之外的其它成分。
限选实验试剂:蒸馏水、6mol·L-1H2SO4溶液、6mol·L-1NaOH溶液、6mol·L-1氨水、0.01mol·L-1KMnO4溶液、新制氯水、20%KSCN溶液。
| 实验步骤 | 预期实验现象和结论 |
| 步骤1:将反应所得浊液过滤、洗涤,取少量固体于试管中,加入足量的6mol·L-1 H2SO4溶液,充分振荡,静置。 | ___________________________________, 证明黑色固体含有Si |
| 步骤2:
|
滤去不溶物(不考虑可溶物的损失),配成250mL溶液,取出25.00mL溶液,按下列操作进行实验:

在上述操作中,需要用到的玻璃定量仪器有________________________________;
计算黑色固体中Al的质量分数为__________________(相对原子质量:Al-27 Fe-56 H-1 O-16)。
(1)大于(2分) (2)②4Al+3SiO23Si+2Al2O3(3分) (3)Fe、Si(2分)
(4)
| 步骤1: | 有气体放出,黑色固体部分溶解(1分) |
| 步骤2:取A试管中少量上层清夜,加入少量新制氯水,再滴加1~2滴20%KSCN溶液(2分) (或其他合理答案) | 溶液显红色,证明黑色固体含有Fe(1分) |
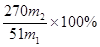 (3分)
(3分)(1)等量的铝消耗的盐酸多于氢氧化钠的,所以盐酸中剩余的铝多。
(2)铝和二氧化硅的反应是置换反应,反应式为4Al+3SiO23Si+2Al2O3。
(3)根据假设1、2可知,假设3应是Al和Fe、Si。
(4)由于铁能和酸反应,硅不能。但硅能和氢氧化钠溶液反应,而铁不能,据此可以鉴别。
(5)配制一定物质的量浓度溶液需要容量瓶,溶液显碱性,准确量取溶液需要碱式滴定管。最后得到的固体是氧化铝,黑色固体中Al的质量分数为