问题
计算题
(6分)一包氯化镁和硫酸钠组成的混合物中,为测定其中氯化镁的的质量分数,小亮同学称取该混合物样品20g,完全溶于水中,然后取用了一定溶质质量分数的氢氧化钠溶液100g,平均分四次加入其中,充分振荡后,测得实验数据如下表所示,请分析并进行相关的计算:
| 次数 | 1 | 2 | 3 | 4 |
| 加入氢氧化钠溶液的质量(g) | 25 | 25 | 25 | 25 |
| 生成沉淀的质量(g) | 2.9 | X | 8.7 | 8.7 |
⑵试求原固体混合物样品中氯化镁的质量分数是 。
答案
⑴ 5.8(2分); ⑵ 71.25%
(1)根据实验1和3可知,25g氢氧化钠溶液就生成2.9g沉淀,所以在实验2中应该生成5.8g沉淀。
(2)根据实验3、4可知,沉淀的最大值是8.7g,即氢氧化镁是8.7g,所以根据方程式2NaOH+MgCl2=Mg(OH)2↓+2NaCl可知,氯化镁的质量是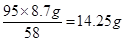 ,所以原固体混合物样品中氯化镁的质量分数是
,所以原固体混合物样品中氯化镁的质量分数是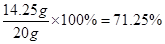 。
。
