探究是一种重要的学习方式,是充分理解学科本质的基本途径.在加热氯酸钾和二氧化锰制取氧气的过程中,鉴于制得的氧气中有氯气的气味,化学兴趣小组的同学通过查阅资料,认为反应过程如下:
①2KClO3+2MnO2
2A+Cl2↑+B↑ △ . .
②2A
K2MnO4+MnO2+B↑ △ . .
③Cl2+K2MnO4
2KCl+MnO2+B↑ △ . .
请写出A、B的化学式:A______B______.通过以上实例,谈谈你对二氧化锰作催化剂的认识______.
如图是同学们在探究氧气性质实验中改进的实验装置图,你认为乙装置中加入的液体是______;
简要回答甲、乙两个集气瓶中液体的作用______.
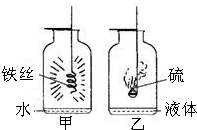
根据质量守恒定律,反应前后各元素的原子个数相等,分析化学方程式①②③,则推断出A、B的化学式分别是KMnO4、O2;通过分析化学方程式①②③知二氧化锰参与了化学反应,反应前后其质量和化学性质不变.同学们在探究氧气性质实验中改进了实验装置图,乙装置中硫燃烧能生成二氧化硫气体有毒,所以乙装置中加入的液体是 氢氧化钠溶液(或氢氧化钾溶液等可溶性碱溶液).甲图中生成的四氧化三铁温度较高,所以防止生成物熔化后溅落到集气瓶底部,使集气瓶破裂,而乙图中生成有毒的二氧化硫,所以应该吸收防止污染大气.甲、乙两个集气瓶中液体的作用是:吸收燃烧产物,防止二氧化硫污染空气.
故答案为:KMnO4、O2;二氧化锰参与了化学反应,反应前后其质量和化学性质不变;氢氧化钠溶液(或氢氧化钾溶液等可溶性碱溶液);防止生成物熔化后溅落到集气瓶底部,使集气瓶破裂;吸收燃烧产物,防止二氧化硫污染空气.
