铝土矿(主要成分为Al2O3,还有少量杂质)是提取氧化铝的原料。提取氧化铝的工艺流程如下:

(1)请用离子方程式表示以上工艺流程中第①步反应:_______ _______。
(2)写出以上工艺流程中第③步反应的化学方程式:______ ___________。
(3)金属铝与氧化铁混合在高温下,会发生剧烈的反应。该反应的化学方程式_____________。请举一例该反应的用途________________。
(4)电解熔融氧化铝制取金属铝,若有0.9mol电子发生转移.理论上能得到金属铝的质量是________________。
(1)Al2O3+2OH-=2AlO2-+H2O
(2)NaAlO2+CO2+2H2O=Al(OH)3↓+NaHCO3
(3)2Al+Fe2O3 2Fe+Al2O3: 焊接铁轨
2Fe+Al2O3: 焊接铁轨
(4)8.1g
题目分析:(1)因题目已经给出了铝土矿的主要成分是Al2O3,所以第一步反应中与NaOH溶液反应的是Al2O3,Al2O3+2OH-=2AlO2-+H2O
(2)结合实验室制取Al(OH)3的原理,我们可以写出反应方程式NaAlO2+CO2+2H2O=Al(OH)3↓+NaHCO3
(3)铝热反应方程式:2Al+Fe2O3=2Fe+Al2O3。
(4)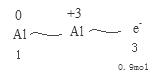
所以可以推出反应的铝为0.3mol,质量为0.3mol*27g/mol=8.1g
