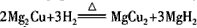氢气是一种清洁能源,氢气的制取与储存是氢能源利用领域的研究热点。已知:
CH4(g)+ H2O(g)==== CO(g)+3H2(g) △H =206.2kJ·mol-1
CH4(g)+ CO2(g)==== 2CO(g)+2H2(g)△H =247.4kJ·mol-1
2H2S(g)====2H2(g)+S2(g) △H =169.8kJ·mol-1
(1)以甲烷为原料制取氢气是工业上常用的制氢方法。CH4(g)与H2O(g)反应生成CO2(g)和H2(g)的热化学方程式为_____________________。
(2)H2S热分解制氢时,常向反应器中通入一定比例空气,使部分H2S燃烧,其目的是__________________________;燃烧生成的SO2与H2S进一步反应,生成物在常温下均非气体,写出该反应的化学方程式:
_____________________。
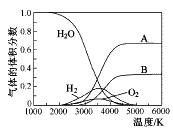
(3)H2O的热分解也可得到H2,高温下水分解体系中主要气体的体积分数与温度的关系如图所示。图中A、B表示的物质依次是______________。
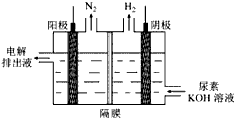
(4)电解尿素[CO(NH2)2]的碱性溶液制氢的装置示意图见下图(电解池中隔膜仅阻止气体通过,阴、阳极均为惰性电极)。电解时,阳极的电极反应式为__________________。
(5)Mg2Cu是一种储氢合金。350℃时,Mg2Cu与H2反应,生成MgCu2和仅含一种金属元素的氢化物(其中氢的质量分数为0.077)。Mg2Cu与H2反应的化学方程式为______________________。
(1)CH4(g)+2H2O(g)==CO2(g)+4H2(g) △H = 165.0 kJ·mol-1
(2)为H2S热分解反应提供热量;2H2S+SO2==2H2O+3S↓(或4H2S+2SO2==4H2O+3S↓)
(3)H、O(或氢原子、氧原子)
(4)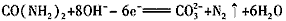
(5)