将镁、铝的混合物7.8 g溶于100 mL 6 mol/L的H2SO4溶液中,然后再滴加2 mol/L的NaOH溶液。请回答:
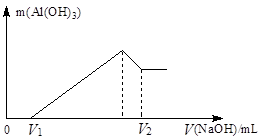
(1)若在滴加NaOH溶液的过程中,沉淀质量随加入NaOH溶液的体积V变化如下图所示。当V1=200 mL时,则金属粉末中,n(Mg)=_________mol,V2=__________mL。
(2)若在滴加NaOH溶液的过程中,欲使Mg2+、A13+刚好沉淀完全,则滴入NaOH溶液的体积为__________mL。
(本题5分)(1)0.1 700 (2)600
题目分析:(1)由图像可知:V1 mL的NaOH溶液是与过量H2SO4反应的,则与Mg、
Al反应的为H2SO4的物质的量是0.6mo-2mol×0.2L÷2=0.4mol
设混合物中镁和铝的物质的量n(Mg)=x mol,n(Al)=y mol
则x+1.5y=0.4mol、24x+27y=7.8g
解得x=0.1mol、y=0.2mol
当加入V2 mL NaOH溶液时,得到Mg(OH)2沉淀和NaAlO2
关系式为: Mg2+~2OH-,Al3+~4OH-,
则V2=200 mL+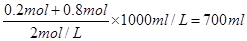
(2)当Mg2+、Al3+刚好沉淀完全时,溶液中只有Na2SO4
关系式为2NaOH~H2SO4
则滴入NaOH溶液的体积为V(NaOH)=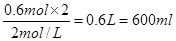
点评:该题是中等难度的试题,试题贴近高考,基础性强,难易适中,侧重对学生能力对培养和解题方法的指导与训练,有利于培养学生的逻辑推理能力和规范的答题能力。也有助于提升学生的学科素质,提高学生分析问题、解决问题的能力。该题的关键是明确反应的原理,然后结合图像信息具体问题、具体分析即可。
