(14分)铁、铝、铜、硅及其合金材料在生产生活中有着广泛的应用。请回答下列有关问题。
(1)目前已冶炼出纯度达99.9999%的铁。下列关于纯铁的叙述错误的是
(填字母)。
A.硬度比钢小,熔点比钢高
B.不能与盐酸反应
C.与不锈钢成分相同
D.在冷的浓硫酸中钝化E.在潮湿的空气中放置不易生锈
(2)铝热反应可用于焊接钢轨、冶炼熔点较高的金属。请写出用V2O5冶炼钒的化学方程式:
(3)①铜在干燥的空气中性质稳定,在潮湿的空气里会被锈蚀形成一层绿色的铜锈,反应的化学方程式是
②工业上常以黄铜矿为原料,采用火法溶炼工艺生产铜。该工艺的中间过程会发生反应:2Cu2O+Cu2S 6Cu+SO2↑,该反应的氧化剂是
6Cu+SO2↑,该反应的氧化剂是
③将铜粉放入稀硫酸中加热并不断鼓入空气,铜溶解,产物只有硫酸铜与水 。
该反应的化学方程式: ,
此法比直接用浓硫酸与铜反应有两个明显的优点:
。
(4)制备高纯硅的流程如下图:

写出石英砂制备粗硅的化学方程式:
。
(14分,每空2分)(1)BC
(2)10Al+3V2O5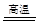 10V+5Al2O3
10V+5Al2O3
(3)①2Cu+O2+H2O+CO2=Cu2(OH)2CO3
② Cu2O、Cu2S
③2H2SO4+2Cu+O2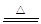 2CuSO4+2H2O
2CuSO4+2H2O
制取相同量的硫酸铜消耗硫酸少;不产生有毒气体
(4)2C+SiO2 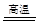 Si+2CO
Si+2CO
题目分析:(1)A、纯铁比合金的熔点高,硬度小,正确;B、能与盐酸反应,错误;C、不锈钢的成分中除含铁外,还含有非金属碳,成分不同,错误;D、铁在冷的浓硫酸中发生钝化,正确;E、高纯铁因为不含碳,即使在潮湿空气中也不易形成原电池而生锈,正确,答案选BC;
(2)V2O5与Al反应冶炼钒,化学方程式是10Al+3V2O5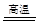 10V+5Al2O3
10V+5Al2O3
(3)①铜与空气中的氧气、水、二氧化碳反应生成碱式碳酸铜,化学方程式为2Cu+O2+H2O+CO2=Cu2(OH)2CO3
②氧化还原反应中氧化剂是指元素化合价降低,得电子的物质,2Cu2O+Cu2S 6Cu+SO2↑中,元素化合价降低的是Cu,所以氧化剂是Cu2O、Cu2S;
6Cu+SO2↑中,元素化合价降低的是Cu,所以氧化剂是Cu2O、Cu2S;
③铜与氧气、稀硫酸在加热条件下反应生成硫酸铜和水,化学方程式为2H2SO4+2Cu+O2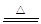 2CuSO4+2H2O;此法比直接用浓硫酸与铜反应有两个明显的优点:制取相同量的硫酸铜消耗硫酸少;不产生有毒气体而污染空气;
2CuSO4+2H2O;此法比直接用浓硫酸与铜反应有两个明显的优点:制取相同量的硫酸铜消耗硫酸少;不产生有毒气体而污染空气;
(4)石英砂的主要成分是二氧化硅,与碳在高温条件下反应生成硅单质和一氧化碳,化学方程式:
2C+SiO2 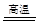 Si+2CO
Si+2CO
