(1)现有如下两个反应:
(A)NaOH+HCl=NaCl+H2O(B)2FeCl3+Cu=2FeCl2+CuCl2
①根据两反应本质判断,______能设计成原电池(填“A”或“B”).
②如果(A或B)不能,说明其原因______.
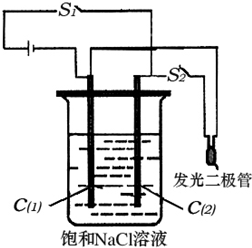
(2)如图所示装置,烧杯中盛有滴有酚酞的NaCl饱和溶液,C(1)、C(2)为多孔石墨电极.
①接通S1后,两极均有气体生成,C(1)附近溶液显______色.装置内发生的总反应化学方程式为______.
②若有11.7g NaCl发生反应,理论上生成Cl2的体积(标准状况)为______.
③反应一段时间后(电极未脱离液面),断开S1,接通S2,观察到二极管发光.此时:C(2)的电极反应式是______.
(1)原电池为自发的氧化还原反应,将化学能转变为电能的装置,NaOH+HCl=NaCl+H2O为中和反应,没有电子转移,不能用来设计原电池,2FeCl3+Cu=2FeCl2+CuCl2为氧化还原反应,可用来设计成原电池,
故答案为:①B; ②A的反应非氧化还原反应,没有电子转移;
(2)①接通S1后,为电解池装置,电解饱和食盐水,阳极反应为2Cl--2e-=Cl2↑,阴极反应为2H2O+2e-=2OH-+H2↑,总化学方程式为2NaCl+2H2O
H2↑+Cl2↑+2NaOH, 电解 .
C(1)连接电源负极,为电解池阴极,生成大量的OH-,滴加酚酞变红色,
故答案为:红色;2NaCl+2H2O
H2↑+Cl2↑+2NaOH; 电解 .
②n(NaCl)=
=0.2mol,根据反应2NaCl+2H2O11.7g 58.5g/mol
H2↑+Cl2↑+2NaOH可知,生成n(Cl2)=0.1mol, 电解 .
则:V(Cl2)=0.1mol×22.4L/mol=2.24L,故答案为:2.24L;
③断开S1,接通S2,为原电池装置,各电极反应与电解池相反,C(2)的电极反应式是Cl2+2e-═2Cl-,
故答案为:Cl2+2e-═2Cl-.
