Na2CO3和H2O2结合成棒状晶体,Na2CO3·xH2O2(过氧化氢合相当于水合。注意:使用高浓度H2O2时一定要小心,防止爆炸生成水和氧气),可消毒、漂白或作O2源…。现称取一定质量的Na2CO3·xH2O2晶体加热。实验结果以温度和相对质量分数示于下图。
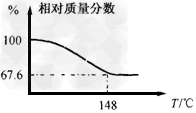
(1)该棒状晶体的化学式Na2CO3·xH2O2中x=_____________。
(2)加热过程中,在141℃时表现为放热,其原因可能是:_______________
a. Na2CO3·xH2O2分解放热
b. 产生的H2O2分解放热
c. Na2CO3·xH2O2分解吸收热量小于产生的H2O2分解放出的热量
(3)事实上,Na2CO3·H2O2(x=1时)是Na2CO4·H2O(Na2CO4叫做过氧碳酸钠)。洗衣粉中加入适量的Na2CO4可以提高洗涤质量,其目的是对衣物进行漂白、消毒。试用化学方程式表示上述洗涤原理______________________。
(4)写出Na2CO4溶液与稀硫酸反应的离子方程式__________________。
(5)下列物质不会使过碳酸钠失效的是_____________
A、 MnO2 B、H2S C、CH3COOH D、NaHCO3
(6)Na2O2、K2O2、CaO2以及BaO2都可与酸作用生成过氧化氢,目前实验室制取过氧化氢的水溶液可通过上述某种过氧化物与适量稀硫酸作用,最适合的过氧化物是___________,原因是_______________。要使获得的过氧化氢从其水溶液中分离出来,采取的措施是___________________ 。
(7)写出过氧酸根的等电子体____________________(一到二种)
(1)x=1.5
(2)c
(3)2Na2CO4=2Na2CO3+O2↑
(4)2CO42-+4H+=2CO2↑+O2↑+H2O
(5)D
(6)BaO2;生成过氧化氢和硫酸钡沉淀,滤去沉淀即得较为纯净的过氧化氢水溶液;减压蒸馏
(7)F2、Br2、I2、ClO-、BrO-、IO- (任意一到两种即可)
