已知:有机物A的产量可以用来衡量一个国家的石油化工发展水平.现以A为主要原料合成乙酸乙酯,其合成路线如下图所示.
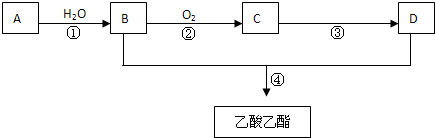
(1)A分子中官能团的名称是______,反应①的化学反应类型是______反应.
(2)反应②的化学方程式是______,
反应④的化学方程式是______.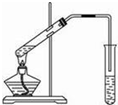
(3)某同学用如图所示的实验装置制取少量乙酸乙酯.实验结束后,试管甲中上层为透明的、不溶于水的油状液体.
①实验开始时,试管甲的导管不伸入液面下的原因是______.
②若分离出试管甲中该油状液体需要用到的仪器是______(填序号).
a.漏斗b.分液漏斗c.长颈漏斗
③实验结束后,若振荡试管甲,会有无色气泡生成,其主要原因是______(结合化学方程式回答).
有机物A的产量可以用来衡量一个国家的石油化工发展水平,则A是乙烯,乙烯和水反应生成乙醇,则B是乙醇,乙醇被氧气氧化生成C,C反应生成D,D和乙醇反应生成乙酸乙酯,则D是乙酸,C是乙醛.
(1)A乙烯,则A中的官能团是碳碳双键,乙烯和水发生加成反应生成乙醇,所以反应类型是加成,故答案为:碳碳双键;加成;
(2)在铜作催化剂、加热条件下,乙醇被氧气氧化生成乙醛和水,反应方程式为2CH3CH2OH+O2
2CH3CHO+2H2O,在浓硫酸作催化剂、加热条件下,乙酸和乙醇发生酯化反应生成乙酸乙酯,反应方程式为CH3COOH+C2H5OH△Cu
CH3COOC2H5+H2O,浓H2SO4 △
故答案为:2CH3CH2OH+O2
2CH3CHO+2H2O;CH3COOH+C2H5OH△Cu
CH3COOC2H5+H2O;浓H2SO4 △
(3)①生成物含有乙醇和乙酸,二者都易溶于水,不能用插入到液面以下,否则产生倒吸现象,故答案为:防止溶液倒吸;
②生成的乙酸乙酯不溶于饱和碳酸钠溶液,应用分液的方法分离,故答案为:b;
③乙酸易挥发,具有酸性,可与碳酸钠发生2CH3COOH+Na2CO3=2CH3COONa+H2O+CO2↑,产生气泡,
故答案为:乙酸的沸点低,加热时,少量乙酸进入试管甲,振荡时,乙酸与碳酸钠接触,发生反应2CH3COOH+Na2CO3=2CH3COONa+H2O+CO2↑,产生气泡.
