18.4 g NaOH 和 NaHCO3固体混合物,在密闭容器中加热到约 250℃,经充分反应后排出气体,冷却,称得剩余固体质量为 16.6 g。试计算原混合物中 NaOH 的质量分数。
54.3%
发生的反应有:①2NaHCO3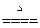 Na2CO3+H2O+CO2↑,
Na2CO3+H2O+CO2↑,
②2NaOH+CO2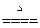 Na2CO3+H2O(加热条件下,不生成 NaHCO3)
Na2CO3+H2O(加热条件下,不生成 NaHCO3)
通过极限思维可知,原固体混合物中,NaHCO3含量越大,固体失重越大,NaOH 含量越大,固体失重越小。
判断 NaHCO3受热分解产生的 CO2能否被 NaOH 完全吸收是解决问题的关键,这首先需要写出 NaHCO3与 NaOH 恰好完全反应的化学方程式。
题设条件下,固体失重:18.4 g-16.6 g =" 1.8" g。
设固体失重 1.8 g 需恰好完全反应的 NaHCO3和 NaOH 混合物质量为 x,则:
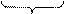 NaHCO3+NaOH
NaHCO3+NaOH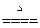 Na2CO3+H2O
Na2CO3+H2O
124 g 18 g
x 1.8 g
x = 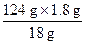 =" 12.4" g<18.4 g
=" 12.4" g<18.4 g
可见,题设条件下反应发生后 NaOH 过量,过量 NaOH 质量为:
18.4 g-12.4 g =" 6.0" g,
参加反应的 NaOH 质量为: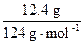 ×40.0 g·mol-1 =" 4.00" g,
×40.0 g·mol-1 =" 4.00" g,
原混合物中 NaOH 质量为:6.0 g+4.00 g =" 10.0" g,
w(NaOH) = 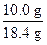 ×100% = 54.3%。
×100% = 54.3%。
答案:54.3% 。
