问题
计算题
在120 ℃时,将12.4 g CO2和H2O(g)的混合气体缓缓通过过量的过氧化钠固体,充分反应之后,固体的质量增加6 g。请计算:
(1)产生氧气的质量。
(2)原混合气体中CO2的质量。
答案
(1)产生氧气的质量为6.4 g。
(2)原混合气体中CO2的质量为8.8 g。
(1)根据质量守恒
m(O2)="12.4" g-6 g="6.4" g
(2)设12.4 g混合气体中含CO2质量为x,则含H2O质量为12.4 g-x。
2Na2O2+2CO2====2Na2CO3+O2
88 32
x 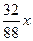
2Na2O2+2H2O====4NaOH+O2↑
36 32
12.4 g-x 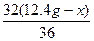
即
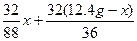 ="6.4" g
="6.4" g
x="8.8" g
